Болезнь Вильсона-Коновалова
Болезнь Вильсона-Коновалова (гепатоцеребральная дистрофия, гепатолентикулярная дегенерация) — это генетическое расстройство, не позволяющая организму удалять лишнюю медь, вызывая накопление меди в печени, головном мозге, глазах и других органах.
Для поддержания здоровья организму требуется небольшое количество меди из пищи, но большое количество меди вредно. Без лечения болезнь Вильсона может привести к высокому содержанию меди, что может привести к опасному для жизни повреждению органов.
Насколько распространена болезнь?
Эксперты все еще изучают, насколько распространена болезнь Вильсона. Более старые исследования показали, что больны примерно 1 из 30 000 человек. Эти исследования были проведены до того, как ученные обнаружили мутации генов, вызывающих заболевание.
Более новые исследования генов пациентов предполагают, что заболевание может быть более распространенной. Исследование, проведенное в Великобритании, показало, что примерно у 1 из 7000 человек есть генетические мутации, вызывающие болезнь Вильсона.
Эксперты не уверены, почему генные исследования предполагают, что заболевание встречается чаще, чем считалось ранее. Одной из причин может быть то, что некоторым больным пациентом не ставили диагнозы. Другая причина может заключаться в том, что некоторые пациенты имеют мутации генов, но заболевание по какой-то причине не развивается.
Причины болезни Вильсона-Коновалова
Как известно, болезнь Вильсона вызывают мутации гена под названием ATP7B. Эти мутации генов не позволяют организму удалить лишнюю медь из организма. Обычно печень выделяет лишнюю медь в желчь. Медь вместе с другими токсичными веществами и отходами выводится из организма через желудочно-кишечный тракт. При заболевании печень выделяет меньше меди в желчь, соответственно, в организме её остается больше.
Мутации ATP7B, вызывающие заболевание, наследуются, т.е., передаются от родителей ребенку. Мутация является аутосомно-рецессивной, что означает, что ребенок должен унаследовать две мутировавшие копии гена ATP7B, по одному от каждого родителя, чтобы заболеть. Люди, имеющие один ген ATP7B без мутации и один ген ATP7B с мутацией, обычно не страдают заболеванием, а являются её носителями.
Людям может быть присуща болезнь, если оба родителя являются носителями, не страдающими от неё сами. На приведенной ниже диаграмме показана вероятность наследования заболевания от родителей, которые являются носителями.

Мутации, вызывающие болезнь Вильсона, являются аутосомно-рецессивными, что означает, что человек должен унаследовать две копии гена с мутациями, чтобы заболеть.
Симптомы болезни Вильсона
Симптомы болезни Вильсона многообразны. Состояние присутствует при рождении, но симптомы не проявятся, пока не накопиться слишком много меди в печени, головном мозге или других органах.
Некоторые пациенты не испытывают признаков и симптомов гепатоцеребральной дистрофии до постановления диагноза и лечения. Однако, если симптомы присутствуют, они связаны с печенью, нервной системой и психическим здоровьем, глазами или другими органами.
Печеночные симптомы

У людей с болезнью Вильсона могут развиться признаки гепатита или воспаление печени. В некоторых случаях эти симптомы у больных появляются, когда возникает острая печеночная недостаточность.Симптомы включают:
- чувство усталости;
- тошнота и рвота;
- отсутствие аппетита;
- боль над печенью, в верхней части живота;
- потемнение цвета мочи;
- светловатый цвет стула;
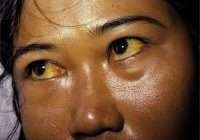
- желтоватый оттенок склер глаз и кожи (желтуха)
Некоторые люди с заболеванием имеют симптомы только в том случае, если у них развивается хроническая болезнь печени и осложнения, вызванные циррозом печени. Эти симптомы могут включать:
- чувство усталости или слабости;
- беспричинное похудение;
- вздутие живота от скопления жидкости в животе (асцит);
- отек голеней, лодыжек или ступней;
- зуд кожи;
- желтуху.
Признаки со стороны нервной системы и психического здоровья
У пациентов с заболеванием могут развиться проблемы с нервной системой и психическим здоровьем. Эти проблемы чаще встречаются у взрослых, но иногда появляются и у детей. Симптомы нервной системы могут включать:
- проблемы с речью, глотанием или физической координацией;
- скованность мышц;
- тремор или неконтролируемые движения.
Симптомы психического здоровья могут включать:
- тревогу;
- изменения в настроении, личности или поведении;
- депрессию;
- психоз.
Глазные симптомы

Многие люди с болезнью Вильсона имеют кольца Кайзера-Флейшера, представляющие собой кольца зеленоватого, золотого или коричневатого цвета по краям роговицы. Кольца появляется в результате накопление меди в глазах. Так просто их не заметить, обычно врач-офтальмолог обнаруживает кольца во время специального обследования глаз, называемого осмотром щелевой лампой.
Среди пациентов с проблемами нервной системы при болезни Вильсона-Коновалова более 9 из 10 имеют кольца Кайзера-Флейшера, а среди больных, испытывающих проблемы с печенью, только 5-6 из 10 имеют кольца Кайзера-Флейшера.
Другие симптомы и проблемы со здоровьем
Гепатоцеребральная дистрофия может повлиять и на другие части тела, вызывая симптомы или проблемы со здоровьем, в том числе:
- тип анемии, называемой гемолитическая анемия;
- проблемы с костями и суставами, например, артрит или остеопороз;
- проблемы с сердцем, например, кардиомиопатия;
- проблемы с почками (ацидоз почечных канальцев и нефролитиаз).
У больных с гепатоцеребральной дистрофией симптомы обычно появляются в возрасте от 5 до 40 лет. Однако у некоторых пациентов признаки проявляются в более молодом или старшем возрасте. Врачи обнаружили первые симптомы болезни Вильсона у детей в возрасте 9 месяцев и у взрослых старше 70 лет.
Диагностика

Болезнь диагностируют на основании медицинской и семейной истории, физического осмотра, осмотра глаз и анализов.
Врачи обычно используют анализ крови и 24-часовой анализ мочи для диагностики болезни Вильсона. Специалисты также проводят биопсию печени и визуализационные исследования.
Медицинская и семейная история.
Врач спросит о семье и личной истории болезни Вильсона и других состояниях, вызывающих симптомы.
Во время медицинского осмотра врач проверит признаки повреждения печени, например:
- изменения кожи;
- увеличение селезенки или печени;
- припухлость на животе;
- отек в нижней части ног, ступней или лодыжек;
- желтоватый цвет белых глаз.
Обследование глаз проводиться щелевой лампой. Во время обследования щелевой лампой врач использует специальный свет для поиска колец Кайзера-Флейшера в глазах.
Для анализа крови медицинский работник возьмет образец крови и отправит ее в лабораторию.
Специалист может заказать один или несколько анализов крови, включая анализы, проверяющие количество:
- церулоплазмина, белка, несущего медь в крови. Люди с болезнью Вильсона часто имеют низкий уровень церулоплазмина, но не всегда.
- меди. У пациентов с заболеванием уровень меди в крови может быть ниже нормы. Острая печеночная недостаточность из-за болезни Вильсона приводит к повышению уровня меди в крови.
- аланинатрансаминаза (АЛТ) и аспартататрансаминаза (АСТ). Больные с гепатоцеребральной дистрофией могут иметь ненормальные уровни АЛТ и АСТ.
- эритроцитов для поиска признаков анемии.
Врачи также могут заказать анализ крови на наличие мутаций гена, вызывающих болезнь, если другие медицинские анализы не помогут подтвердить или исключить диагноз заболевания.
24-часовой анализ мочи.
В течение 24 часов пациент должен будет собирать свою мочу в домашних условиях в специальный контейнер, предоставив ее потом медицинским работникам. Медицинский работник отправит мочу в лабораторию, которая проверит количество меди в моче. Уровень меди в моче у пациентов с болезнью Вильсона-Коновалова часто выше нормы.
Если результаты анализов крови и мочи не подтверждают или не исключают диагноз заболевания, врач назначит биопсию печени. Во время биопсии врач извлечет небольшие кусочки ткани из печени, а патологоанатом исследует ткань под микроскопом, чтобы найти особенности конкретных заболеваний печени, такие как болезнь Вильсона, и проверит наличии повреждений и цирроза печени. Кусочек ткани печени будет отправлен в лабораторию, которая проверит количество меди в ткани.
Визуализационные методы исследования.
При проблемах с нервной системой врачи могут заказать визуальные тесты для выявления признаков болезни Вильсона или других состояний мозга.
- Магнитно-резонансная томография (МРТ), которая использует радиоволны и магниты для получения детальных изображений органов и мягких тканей без использования рентгеновских лучей.
- Компьютерная томография (КТ), которая использует комбинацию рентгеновских лучей и компьютерных технологий для создания детальных изображений.
Лечение болезни Вильсона-Коновалова
Лечат заболевание при помощи:
- лекарств, удаляющих медь из организма, называемых хелатирующими агентами;
- цинка, препятствующего поглощению меди кишечником.
Во многих случаях лечение улучшает или предотвращает симптомы и повреждения органов. Врачи также могут порекомендовать изменить диету, чтобы избежать употребления продуктов с высоким содержанием меди.
Люди с болезнью Вильсона-Коновалова нуждаются в пожизненном лечении. Прекращение терапии может привести к острой печеночной недостаточности. Медицинские работники регулярно будут проводить анализы крови и мочи, чтобы проверять, как протекает лечение.
Хелатирующие агенты
Пеницилламин (Купрамин, Депен) и Триентин (Сиприн) являются двумя хелатирующими агентами, используемыми для лечения болезни Вильсона. Лекарства удаляют медь из организма.
Пеницилламин чаще вызывает побочные эффекты, чем триентин. Побочные эффекты пеницилламина могут включать лихорадку, сыпь, проблемы с почками или проблемы с костным мозгом. Пеницилламин также снижает активность витамина В6, поэтому врачи могут порекомендовать принимать добавку витамина В6 вместе с пеницилламином. В некоторых случаях, когда пациенты с симптомами нервной системы начинают принимать хелатирующие агенты, их симптомы усиливаются.
Когда начинается лечение, врачи постепенно увеличивают дозу хелатирующих агентов. Больные принимают более высокие дозы хелатирующих агентов, пока лишняя медь из организма не будет удалена. Когда симптомы болезни Вильсона улучшатся, и анализы покажут, что содержание меди на безопасном уровне, могут назначить более низкие дозы хелатирующих агентов в качестве поддерживающей терапии. Препараты этой группы применяются с перерывами в течение всей жизни.
Хелатирующие агенты могут мешать заживлению ран, поэтому, на момент операции врачи могут назначать более низкие дозы препарата.
Цинка предотвращает поглощение меди кишечником. Врачи могут назначить цинк в качестве поддерживающей терапии, после того, как хелатообразующие агенты удалят лишнюю медь из организма. Также цинк может назначаться людям, у которых болезнь Вильсона-Коновалова обнаружена, но протекает бессимптомно.
Наиболее распространенным побочным эффектом цинка является расстройство желудка.
Прекращение приема лекарств от болезни может вызвать быстрое накопление меди и опасные для жизни последствия. Важно, чтобы пациенты, принимающие ацетат цинка, использовали рецептурную версию этого препарата, потому что пищевые добавки не могут быть биоэквивалентными и могут быть неэффективными.
Питание

Во время лечения, врач может порекомендовать избегать продуктов с высоким содержанием меди, например:
- шоколад;
- печень;
- грибы;
- орешки;
- моллюск.
После того, как лечение понизило уровень меди и началась поддерживающая терапия, поговорите с врачом о том, можно ли безопасно есть умеренное количество этих продуктов.
Если водопроводная вода поступает из колодца или течет по медным трубам, проверьте уровень меди в воде. Вода, проходящая в медных трубах, может содержать медь. Возможно, придется использовать фильтры для воды, чтобы удалить медь из водопроводной воды.
Из соображений безопасности поговорите с врачом перед использованием пищевых добавок, витаминов, или любых дополнительных или альтернативных лекарств. Некоторые пищевые добавки могут содержать медь.
Как лечат болезнь Вильсона беременным женщинам?
Беременные женщины должны продолжать лечение болезни на протяжении всей беременности. Врачи назначат более низкие дозы хелатирующих препаратов. Поскольку плод нуждается в небольшом количестве меди, снижение дозы может удерживать медь на безопасном уровне без удаления слишком большого количества.
В большинстве случаев врачи рекомендуют женщинам продолжать принимать полную дозу цинка во время беременности. Эксперты рекомендуют женщинам с болезнью Вильсона не кормить грудью, если принимают хелатирующие препараты. Пеницилламин присутствует в грудном молоке и может быть вредным для ребенка. О безопасности триентина и цинка, содержащегося в грудном молоке имеется мало информации.
Как лечат осложнения болезни?
Если заболевание приводит к циррозу, врачи лечат проблему и осложнения, связанные с циррозом, с помощью лекарств, операции и других медицинских процедур.
Если болезнь вызывает острую печеночную недостаточность или печеночную недостаточность вследствие цирроза, может потребоваться пересадка печени. Пересадка печени избавляет от заболевания в большинстве случаев.
Профилактика
Предотвратить заболевание нельзя. Если есть родственник первой степени — родитель, брат, сестра — с болезнью Вильсона-Коновалова, поговорите с врачами об обследовании вас и других членов семьи на предмет заболевания. Врач может поставить диагноз и начать лечение до появления симптомов и осложнений.
Ранняя диагностика и лечение могут уменьшить или предотвратить повреждение органов.
Прогноз
Прогноз улучшается при назначении адекватной терапии на ранних стадиях заболевания. Терапия на поздней стадии существенно не влияет на развитие и прогрессирование осложнений и на прогноз заболевания. Смерть наступает преимущественно в молодом возрасте, как правило, от осложнений цирроза печени (кровотечение из варикозно расширенных вен пищевода и желудка, печеночная недостаточность, фульминантная печеночно-клеточная недостаточность), реже — от осложнений, связанных с поражением нервной системы.
Болезнь Вильсона ( Болезнь Вестфаля-Вильсона-Коновалова , Болезнь Вильсона-Коновалова , Гепатолентикулярная дистрофия , Гепатоцеребральная дистрофия , Лентикулярная прогрессирующая дегенерация )
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФазы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Болезнь Вильсона может протекать в брюшной, ригидно-аритмогиперкинетической, дрожательной или экстрапирамидно-корковой форме. Диагностика болезни Вильсона включает офтальмологическое обследование, биохимические анализы мочи и крови, МРТ или КТ головного мозга. Основу патогенетической терапии составляют тиоловые препараты, которые могут приниматься в течении нескольких лет и даже пожизненно.
МКБ-10
Общие сведения
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФ-азы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Первооткрыватель заболевания — А.К. Вильсон, описавший заболевание в 1912 году, в отечественной медицине — Н.А. Коновалов. Патогенез болезни Вильсона был выявлен в 1993 году. Понятию «болезнь Вильсона» соответствуют также: болезнь Вильсона-Коновалова, болезнь Вестфаля-Вильсона-Коновалова, дистрофия гепатоцеребральная, дистрофия гепатолентикулярная, дегенерация лентикулярная прогрессирующая.

Причины
Ген АТР7В картирован на длинном плече хромосомы 13 (13q14.3-q21.1). Организм человека содержит около 50-100 мг меди. Суточная потребность меди для человека — 1-2 мг. 95% абсорбированной в кишечнике меди, транспортируется в форме комплекса с церулоплазмином (один из глобулинов сыворотки, синтезируемых печенью) и только 5% в форме комплекса с альбумином. Кроме того, ион меди входит в состав важнейших метаболических ферментов (лизилоксидаза, супероксиддисмутаза, цитохром-С-оксидаза и др.). При болезни Вильсона происходит нарушение двух процессов обмена меди в печени — биосинтез главного медьсвязывающего белка (церулоплазмина) и выведение меди с желчью, следствием чего становится повышение уровня несвязанной меди в крови. Концентрация меди в различных органах (чаще всего в печени, почках, роговице и головном мозге) увеличивается, что приводит к их токсическому поражению.
Классификация
Согласно классификации Н.В. Коновалова различают пять форм болезни Вильсона:
- брюшная
- ригидно-аритмогиперкинетическая
- дрожательно-ригидная
- дрожательная
- экстрапирамидно-корковая
Симптомы
Для болезни Вильсона характерен клинический полиморфизм. Первые проявления заболевания могут появиться в детстве, юношестве, в зрелом возрасте и гораздо реже в зрелом возрасте. В 40-50% случаев Болезнь Вильсона манифестирует с поражения печени, в остальных — с психических и неврологических расстройств. С вовлечением в патологический процесс нервной системы обнаруживается кольцо Кайзера-Флейшера.
Брюшная форма развивается преимущественно до 40 лет. Характерный признак — тяжелое поражение печени по типу цирроза печени, хронического гепатита, фульминантного гепатита.
Ригидно-аритмогиперкинетическая форма манифестирует в детском возрасте. Начальные проявления — мышечная ригидность, амимия, смазанность речи, трудности при выполнении мелких движений, умеренное снижение интеллекта. Для этой формы заболевания характерно прогрессирующее течение, с наличием эпизодов обострения и ремиссии.
Дрожательная форма возникает в возрасте от 10 до 30 лет. Преобладающим симптомом является тремор. Кроме того, могут наблюдаться брадикинезия, брадилалия, тяжелый психоорганический синдром, эпилептические приступы.
Экстрапирамидно-корковая форма встречается весьма редко. Ее начало схоже с началом какой-либо из вышеперечисленных форм. Для нее характерны эпилептические припадки, экстрапирамидные и пирамидные нарушения и выраженный интеллектуальный дефицит.
Диагностика
Офтальмологическое исследование с помощью щелевой лампы выявляет кольцо Кайзера-Флейшера. Биохимические исследования мочи обнаруживают повышенную экскрецию меди в суточной моче, а также снижение концентрации церулоплазмина в крови. С помощью визуализационных методов (КТ и МРТ головного мозга) обнаруживают атрофию полушарий большого мозга и мозжечка, а также базальных ядер.
При диагностике болезни Вильсона неврологу необходимо дифференцировать ее от паркинсонизма, гепатоцеребрального синдрома, болезни Геллервордена-Шпатца. Основным дифференциально-диагностическим признаком этих заболеваний является отсутствие характерных для болезни Вильсона кольца Кайзера-Флейшера и расстройств обмена меди. Для подтверждения болезни Вильсона проводится генодиагностика.
Лечение болезни Вильсона
Основой патогенетического лечения является назначение тиоловых препаратов, в первую очередь — D-пеницилламина либо унитиола. Главное преимущество купренила — низкая токсичность и возможность длительного приема при отсутствии побочных эффектов. Его назначают по 0,15 г (1 капсула) в сутки (только после еды), в дальнейшем, в течение 2,5-3 месяцев дозу увеличивают до 6-10 капсул/сутки (оптимальная доза). Лечение D-пеницилламином проводится годами и даже пожизненно с небольшими перерывами (на 2-3 недели) в случае появления побочных эффектов (тромбоцитопения, лейкопения, обострения язвенной болезни желудка и т. д.).
Унитиол назначают в случае непереносимости (плохой переносимости) D-пеницилламина. Длительность одного курса лечения — 1 месяц, после чего лечение приостанавливают на 2,5-3 месяца. В большинстве случаев наступает улучшение общего состояния пациента, а также регресс неврологических симптомов (скованности, гиперкинезов). В случае доминирования гиперкинезов рекомендовано назначение небольших курсов нейролептиков, при ригидности — леводопы, карбидопы, тригексифенидила.
В случае тяжелого течения болезни Вильсона, при неэффективности консервативного лечения за рубежом прибегают к трансплантации печени. При положительном исходе операции состояние пациента улучшается, восстанавливается обмен меди в организме. В дальнейшем лечение пациента составляет иммуносупрессивная терапия. В России на сегодня постепенно внедряется в клиническую практику метод биогемоперфузии с изолированными живыми клетками селезенки и печени (т. н. аппарат «вспомогательная печень). Немедикаментозное лечение состоит в назначении диеты (стол №5) в целях исключения продуктов богатых медью (кофе, шоколад, бобовые, орехи и т. д.).
Прогноз и профилактика
В случае своевременного диагностирования болезни Вильсона и проведения адекватной медьснижающей терапии возможна нормализация общего состояние пациента и обмена меди в организме. Постоянный прием тиоловых препаратов по схеме, назначенной врачом-специалистом, позволяет поддерживать профессиональную и социальную активность пациента.
Для предотвращения рецидивов болезни Вильсона рекомендовано проведение лабораторных исследований крови и мочи пациента несколько раз в год. Необходим контроль следующих показателей: концентрация меди, церулоплазмина и цинка. Кроме того, рекомендовано проведение биохимического анализа крови, общего анализа крови, а также регулярные консультации у терапевта и невролога.
Болезнь Вильсона-Коновалова
Болезнь Вильсона-Коновалова – редкое наследственное заболевание, проявляющееся различными печеночными, неврологическими, психиатрическими, костно-мышечными нарушениями вследствие чрезмерного отложения меди в органах и тканях. Из-за длительного течения и многообразия клинических симптомов относится к числу труднодиагностируемых заболеваний.
Заболевание связано с нарушением метаболизма меди и избыточным ее накоплением в различных органах и тканях. Из-за преимущественно накопления меди в печени и в отделах центральной нервной системы оно проявляется в большей степени симптоматикой поражения печени и центральной нервной системы (ЦНС). Из-за токсического влияния свободной меди приданном заболевании нарушается функция органов зрения (роговицы), почек, желез внутренней секреции, сердца, костной ткани.
Первые описания болезни дали C. Westphal в 1883 г. и в A. Strumpell в 1898 г. Они изучали заболевание, при котором регистрировались признаки многоочагового поражения центральной нервной системы на фоне поражения печени. Патология была названа псевдосклерозом. В 1902-1903 г.г. у данных пациентов по периметру роговицы были обнаружены зеленовато-бурые отложения, которые были названные в честь описавших их авторов — кольца Кайзера–Флейшера.
Однако, целостное и подробное описание патологии было дано английским неврологом Самуэлем Вильсоном в 1912 году. Врач описал морфологические отклонения, которые происходят в организме при данном заболевании – двусторонние изменения чечевицеобразных ядер в головном мозге (лентикулярных ядер в подкорковом веществе головного мозга) в сочетании с циррозом печени. В клинической картине он выделил наличие признаков поражения экстрапирамидной системы, бульбарного синдрома и психических расстройств. Заболевание начинало проявлять себя в молодом возрасте и затем неуклонного прогрессировало. Это позволило Вильсону назвать данную патологию прогрессирующей лентикулярной дегенерацией.
Почти через 40 лет J.N. Cumings (1948) и H.G. Kunkel (1952) выявили у данных больных нарушение обмена меди — накоплением ее в мозговой ткани и гиперсекрециию с мочой из-за дефицита медьсодержащего белка церулоплазмина в плазме крови.
В России изучение болезни связано с именем Н.В.Коновалова. Ему принадлежат заслуги описания в 1960 году основных клинических форм данной патологии и создания подробной классификации заболевания.
Распространенность заболевания среди мужчин и женщин одинаковая. Данная патология редко выявляется до достижения 5-летнего возраста. По данным медицинской статистики, частота встречаемости болезни составляет 1 на 7 000 -10 000 человек. На территории Российской Федерации за 2014 и 2015 гг. болезнь Вильсона-Коновалова была выявлена у 572 и 602 человек соответственно.

Суперфуды в косметике: сочные коктейли для здоровья кожи и волос
Симптомы
Симптомы болезни Вильсона-Коновалова складываются из признаков поражения печени, неврологических и психических расстройств. Первыми у 42% пациентов появляются поражения печени, в четверти всех случаев – уже в детском возрасте. Неврологическая симптоматика болезни Вильсона проявляется, как правило, позже — на втором-третьем десятилетиях жизни.
В большинстве случаев поражение печени имеет длительное течение и без лечения приводит к развитию цирроза. Клинически поражение печени первоначально проявляется диспептическими проявлениями, повышенной утомляемостью, недомоганием, потерей аппетита вплоть до развития анорексии, снижением массы тела, суставными болями, увеличением печени, болью в правом подреберье, развитием желтухи, появлением темной мочи. Иногда заболевание может дебютировать снижением уровня лейкоцитов и тромбоцитов в крови. Клинически это проявляется кровотечениями из десен и повторяющимися носовыми кровотечениями.
Постепенно нарастают признаки функциональной недостаточности печени, формируется ее цирротическое поражение, появляются признаки портальной гипертензии, развиваются асцит и печеночная энцефалопатия. В этот период отмечаются нарастание желтухи, боли в животе, диспепсических расстройств. В биохимическом анализе крови выявляются повышение содержания аминотрансфераз (АСТ, АЛТ), снижение содержания альбумина, повышение содержания гаммаглобулинов, нарушение свертываемости крови. Часто заболевание впервые выявляется уже на стадии декомпенсированного цирроза печени с развитием отечно-асцитического синдрома на фоне варикозно расширенных вен пищевода. В ряде случаев больные погибают от печеночной недостаточности еще до развития неврологической симптоматики.
Концентрация меди в головном мозге и спинномозговой жидкости у пациентов с болезнью Вильсона-Коновалова по сравнению со здоровыми увеличивается в 10 раз. Неврологические признаки могут до поры до времени развиваться постепенно, а затем внезапно выйти на первое место в клинической картине заболевания. Определяются экстрапирамидные нарушения – размашистый тремор конечностей, изменение почерка, тремор головы, нарушение речи и ухудшение памяти. Нарастание неврологических симптомов характеризуется появлением насильственных движений – гиперкинезов в виде непроизвольных стереотипных, ритмических, вычурных движений небольшого объема (атетоз), насильственно плача или смеха. Поражение нервной системы может проявиться дрожанием рук, нарастанием тонуса мускулатуры, переходящим в ее ригидность. Затем развиваются клонические и тонические судороги. Дальнейшее прогрессирование болезни приводит к смене ригидности мышц на миогенные контрактуры и обездвиженность.
Нередки экстрапеченочные и экстраневрологические симптомы болезни Вильсона-Коновалова.
У 1% пациентов болезнь проявляется поражением почек из-за отложения меди в почечных канальцах. Это проявляется выведение с мочой аминокислот, продуктов из распада, глюкозы, мочевой кислоты, кальция, а также снижением почечного кровотока и фильтрации. В редких случаях развиваются пиелонефрит, гломерулонефрит и мочекаменная болезнь. Из-за потери кальция и фосфора при нарушении функции почек развиваются остеопороз, рахит, остеомаляция.
Отложение меди в суставах приводит к развитию остеоартрита.
Нарушения со стороны эндокринной системы могут проявляться в отставании полового развития, появлении гинекомастии у юношей, амeнореи или дисменореи у девушек, развитии ожирения, акромегалии, появлении striae gravidarum — полос на коже живота, как при беременности. В 33% случаев у женщин отмечались гипоплазия эндометрия по смешанному типу и кистозная атрезия фолликулов яичников.
Более, чем у половины пациентов с болезнью Вильсона-Коновалова при ультразвуковом исследовании были выявлены фиброзные изменения клапанов сердца и обнаружены признаки обратного тока крови из-за нарушения функции этих клапанов. В ряде исследований выявлена высокая распространенность гипертрофии левого желудочка.
Со стороны органов зрения обнаруживаются кольца Кайзера-Флейшера и помутнение хрусталика.
Формы
Формы болезни Вильсона-Коновалова с 1983 выделяют бессимптомную, печеночную, церебральную и смешанную форма.
Однако, в нашей стране широко распространена классификация Н.В.Коновалова (1960 г), который выделил 5 форм заболевания.
Брюшная (абдоминальная) форма – преневрологическая стадия болезни, развивается обычно в возрасте 5-17 лет, сопровождается быстрым нарастанием поражения печени в нескольких вариантах, без лечения заканчивающееся летально.
Ригидно-аритмогиперкинетическая (ранняя форма) — развивается в возрасте 7-15 лет, отличается быстрым течением. Клиническая картина характеризуется аритмичными гиперкинезами, мышечной ригидностью, развитием контрактур. Гиперкинезы охватывают различные мышечные группы (конечности, туловище, а также мышцы, ответственные за артикуляцию и глотание) и приводят к изменению позы тела, положения конечностей, дизартрии и дисфагии. Выявляется нарушение интеллекта, появляется нарушение речи, нарушение глотания, судорожный смех и плач. Без лечения заканчивается летально через 2-3 года.
Дрожательно-ригидная форма встречается чаще других в более позднем возрасте (17-25 лет) и имеет более доброкачественное течение. Для этого варианта характерно одновременное развитие ригидности и дрожания с варьированием их соотношения. В ряде случаев регистрируются атетоидные насильственные движения (гиперкинезы в виде непроизвольных стереотипных, ритмических, вычурных движения небольшого объема). Часто отмечаются дисфагия и дизартрия. Без лечения срок жизни таких пациентов составляет 5-6 лет.
Дрожательная форма считается наиболее доброкачественной. Она начинается в возрасте 20-30 лет и протекает довольно медленно в течение10-15 лет и более. Основным клиническим проявлением является дрожание. Мышечный тонус не изменен или снижен. По мере прогрессирования болезни дрожание резко усиливается, становится крупноамплитудным. Ригидность появляется только в конце болезни. Интеллектуальные способности длительное время сохраняются, но по мере прогрессирования болезни, наряду с повышением мышечного тонуса, возникают изменения психики, отличающиеся развитием аффективных расстройств.
Экстрапирамидно-корковая форма встречается реже других форм. Характеризуется присоединением к имеющимся типичным нарушениям остро развивающихся пирамидных парезов и эпилептических припадков, чаще очагового характера, и быстрым прогрессом психических нарушений. Эта форма длится в среднем 6-8 лет и заканчивается летально.
Причины
Основной причиной развития болезни Вильсона-Коновалова является нарушение обмена меди и ее отложение в различных органах и тканях. Токсическое действие меди приводит к нарушению функций органов. Причина нарушения обмена меди — дефект в гене, регулирующем ее обмен (АТР7В). В результате нарушаются два основных процесса — синтез медьсодержащего белка церулоплазмина и выведение меди с желчью. Все это ведет к повышению концентрации меди и ее отложению в органах.
В норме поступающая с пищей медь после усвоения в желудочно-кишечном тракте в комплексе с белками переносится в печень, где соединяется со специальным белком, синтезируемым в печени — церулоплазмином. Церулоплазмин необходим для нормального обмена железа, его всасывания и утилизации, поскольку этот белок участвует в мобилизации железа из клеток ретикулоэндотелиальной системы и переводит железо в трехвалентную форму. Медь также входит в состав супероксиддисмутазы – фермента, участвующего в защите клеток от оксидативного стресса при активации перекисного окисления липидов вследствие повышения уровня токсичных форм кислорода. Медь присутствует в ферменте цитохром С-оксидазе, осуществляющей транспорт электронов. Она необходима для работы V и VIII факторов свертывания крови, содержится в активном центре фермента дофамин-бета-гидроксилазы, которая катализирует реакцию перехода дофамина в норадреналин. Важным медьсодержащим белком является фермент лизилоксидаза, участвующая в образовании поперечных связей коллагена – основного белка, из которого строится костная ткань. Медь участвует в реакциях превращения аскорбиновой кислоты (витамина С).
Ген, ответственный за развитие заболевание был идентифицирован в 1993 г. двумя исследовательскими группами из США и Канады. Установлено, что этот ген кодирует синтез медьтранспортирующей аденозинтрифосфатазы Р-типа (медьтранспортирующую АТФ-азу 7В), и именно мутации в этом гене обусловливают нарушение обмена меди в организме.
В сыворотке крови 95 % меди находится в связанном состоянии с белком церулоплазмином. Включение меди в церулоплазмин происходит в аппарате Гольджи при участии медьтранспортирующей АРФ7В. Эта АТФ-аза 7В играет двоякую функциональную роль в клетках печени: одна из них – участие в биосинтезе путем доставки меди к апоцерулоплазмину внутри аппарата Гольджи, другая – транспорт избытка меди из клетки. В настоящее время известно несколько сотен мутаций в гене АТР7В, из которых более 70 идентифицированы в патогенезе заболевания. Такой широкий спектр повреждений в гене АТР7В и разнообразие их комбинаций находит отражение в полиморфизме клинических проявлений и тяжести течения патологии. Однако, пока убедительных данных о корреляциях «генотип-фенотип» получить не удается.
Наиболее распространенной мутацией в гене АТР7В среди европеоидной расы является мутация 3207C>A (H1069Q), при которой в положении 1069 происходит замена (мутация) аминокислоты гистидина на глутаминовую кислоту с образованием «патологического» фермента. Исследователи обнаруживают эту мутацию у 22-38% больных славян.
Генетически детерминируемое снижение функции медь-транспортирующей АТФ-азы в результате молекулярных дефектов в гене АТР7В приводит к снижению удалению меди из организма и нарушению встраивания меди в церулоплазмин, в результате экскретируется и циркулирует апоцерулоплазмин (белок ненагруженный медью, срок полувыведения которого сокращается вдвое, что и объясняет гипоцерулоплазминемию), а медь накапливается в различных органах и тканях, преимущественно в печени, головном мозге, роговице глаза, почках, обеспечивая полиморфизм клинических появлений болезни Вильсона-Коновалова. Перегруженные медью гепатоциты разрушаются и это приводит к формированию стойкого синдрома цитолиза (гибели клеток).
Тип наследования заболевания аутосомно-рецессивный. Это значит, что для клинического проявления болезни нужно, чтобы ребенок унаследовал измененный ген сразу об обоих родителей. Если же измененный ген будет унаследован только от одного из родителей, то ребенок будет «здоровым носителем» болезни.
В патогенезе болезни ведущая роль принадлежит нарушению баланса между объемом поступившей с пищей меди и ее экскрецией. При болезни Вильсона-Коновалова этот баланс нарушается, содержание свободной (токсичной) меди в крови и тканях возрастает, и ее выделение с мочой увеличивается.
Генетическая гетерогенность (большое количество возможных мутаций) может обусловливать и разнообразие механизмов дефекта экскреции меди: в одних случаях он может возникать из-за аномалии экпрессии гена на разных уровнях регуляции синтеза церулоплазмина, в других – из-за препятствия всасываемости меди в тонком кишечнике, в третьих – из-за нарушения выведения меди с желчью, в четвертых – из-за появления в печени патологически измененного металлотионейона (белок, связывающий медь и другие тяжелые металлы). Это приводит к накоплению в гепатоците так называемой регуляторной фракции меди. Избыточная концентрация последней провоцирует генерацию свободных радикалов, нарушение проницаемости плазматической мембраны и мембран митохондрий, истощение клеточных запасов и, как следствие, повреждение структур гепатоцита. При нарушении выведения меди с желчью при болезни Вильсона-Коновалова она долгое время депонируется в гепатоцитах. Избыток меди ведет к возникновению каскада патобиохимических реакций, вызывая развитие вильсоновского гепатита (гепатоза) с последующим переходом в атрофический нодулярный цирроз печени.
Хотя патогенез болезни еще недостаточно изучен, существует несколько его гипотез, две из которых считаются ведущими.
- Теория генетического дефекта синтеза церулоплазмина, который сопровождается нарушением поступления меди в печень. В результате возврат меди в кровь обеспечивает поступление ее с током крови к органам-мишеням (мозг, сердце, роговица, почки и др.).
- Существуют мнения, что дефект гена, ответственного за синтез церулоплазмина, по-видимому, не является ведущим фактором развития болезни Вильсона-Коновалова, а играет вторичную роль. Первичным звеном развития болезни следует считать изменение метаболизма меди в печени из-за нарушения ее выделения из аппарата Гольджи в желчь. Ионы меди, поступающие в избытке в ткани, очень токсичны и способны окислять белки и липиды клеточных мембран, связывать белки и нуклеиновые кислоты и усиливать синтез свободных радикалов. Эти радикалы окисляют липиды, ферменты и белки цитоскелета. Вследствие повышения внутриклеточной концентрации меди повреждается множество внутриклеточных систем.
Методы диагностики
Диагностика болезни Вильсона-Коновалова проводится обычно врачами гастроэнтерологом, неврологом, офтальмологом, генетиком на основании жалоб, данных анамнеза, клинического осмотра, обязательного применения лабораторных (включая генетические) и инструментальных методов обследования. Диагностика направлена на определение клинической формы заболевания, тяжести состояния и возникающих осложнений.
Из анамнеза можно выяснить наличие эпизодов желтухи, неврологических отклонений, заболеваний печени.
При объективном обследовании могут определяться умеренное увеличение печени и селезенки, признаки желтухи (желтушные склеры), наличие колец Кайзера-Флейшера на роговице.
Как правило наличие болезни не вызывает сомнений при обнаружении снижения в крови белка церулоплазмина, увеличения выведения меди с мочой и наличия колец Кайзера-Флейшера.
При размытых клинических симптомах может потребоваться проведение биопсии печени для определения содержания меди в ее клетках и проведение генетического обследования для обнаружения мутаций в гене АТР7В.
При определении меди в крови следует выделять два понятия – «общая медь» и «свободная медь». Для определения общей меди обычными рутинными методами ее содержание определяют по определения церулоплазмина, белка, который включает 90-95% меди. Поэтому количество общей меди, из-за падения содержания церулоплазмина при болезни Вильсона-Коновалова тоже уменьшается. Для точного подтверждения диагноза в качестве диагностического теста проводят определение несвязанной с церулоплазмином меди (свободной – токсичной) в моче методом масс-спектрометрии. Для установления факта усиления экскреции меди с мочой проводят пробу с пеницилламином. После его введения многократное увеличение меди в моче подтверждает диагноз.
В сыворотке крови также определяется повышение свободной (несвязанной) меди и снижение содержания церулоплазмина. Следует учитывать, что нормальной содержание церулоплазмина не всегда исключает диагноз болезни Вильсона-Коновалова, т.к. в 20% случаев у детей при подтвержденном диагнозе содержание этого белка оставалось в пределах нормы.
В ткани печени (биопсийный материал) определяется повышение содержания меди. У гетерозиготных носителей гена АТР7В (получивших от родителей один мутированный ген) концентрация меди в печени тоже повышена, но в меньшей степени.
При остром течении болезни в крови выявляется увеличение активности трансаминаз (АЛТ и АСТ), увеличение содержания билирубина и повышение содержания уробилина в моче.
При нарушении свойств печени синтезировать белки (синтетической функции) происходят нарушения в свертывающей системы крови, что проявляется снижением протромбинового индекса.
В клиническом анализе крови выявляются признаки анемии, ретикулоцитоз, ускорение СОЭ.
В общем анализе мочи при поражении почек — протеинурия, глюкозурия (наличие глюкозы), увеличение количества аминокислот и их продуктов (аминоацидурия).
Типичным признаком болезни являются кольца Кайзера-Флейшера на роговице глаза, определяющиеся у 55-70% взрослых пациентов. При вовлечении ЦНС это кольцо определяется практически у всех пациентов.
Генетическое исследование подразумевает выявление мутаций в гене АТР7В.
Проводится дородовая (пренатальная) диагностика болезни Вильсона-Коновалова на плодном материале. Следует иметь в виду, что если мутация обнаруживается только на одной из гомологичных хромосом, то достоверно диагноз поставить о наличии болезни нельзя. Диагноз является 100%, если мутация обнаружена в гомозиготном состоянии (в 2-х одинаковых генах в гомологичных хромосомах – ребенок унаследовал 2 мутированных гена).
Инструментальные исследования назначаются для оценки состояния печени (УЗИ печени и желчных протоков, селезенки). При клинических признаках нарушения ЦНС проводят МРТ и КТ головного мозга — обнаруживается атрофия коры и ствола мозга, увеличенные желудочки. При наличии судорожного синдрома и других неврологических признаках показано проведение электроэнцефалографии (ЭЭГ).
Обследование органов зрения, с целью выявления колец Кайзера-Флейшера проводится врачом-офтальмологом при помощи щелевой лампы.
При поражении сердца, почек, костей, эндокринных органов назначаются соответствующие инструментальные обследования (УЗИ почек, ЭКО-КГ и др.).
В пользу правильности диагноза будет свидетельствовать высокий терапевтический эффект при применении медьвыводящих препаратов.
Дифференциальная диагностики проводится в гепатитами неясной этиологии, циррозом печени. При развитии неврологических симптомов с паркинсонизмом.
Основные используемые лабораторные исследования.
- Клинический анализ крови.
- Общий анализ мочи.
- Биохимический анализ крови (включая АСТ, АЛТ, билирубин).
- Исследование свертывания крови.
- Определение меди в суточной моче (Масс-спектрометрия c источником ионов в виде индуктивно связанной плазмы/ИСП-МС).
- Определение меди в крови (колориметрический метод).
- Определение меди в ткани печени (биопсийный материал).
- Поиск 12 наиболее вероятных мутаций в гене АТР7В.
- Пренатальная диагностика болезни Вильсона. (выявление носительства мутаций в гене АТР7В).
Основные используемые инструментальные исследования.
- УЗИ органов брюшной полости (печень, поджелудочная железы, селезенка, почки).
- МРТ и КТ печени, поджелудочной железы, селезенки.
- Эластометрия печени.
- МРТ/КТ головного мозга.
- ЭХО-КГ сердца.
Лечение
Часто болезнь Вильсона-Коновалова диагностируют уже на тяжелой стадии с необратимыми изменениями, и лечение в этом случае уже не ведет к выздоровлению, а лишь к стабилизации патологического процесса.
Патогенетическое лечение направлено на выведение избытка меди и лечение сопутствующих осложнений.
Прогресс в лечении произошел в 1956 году, когда J.M. Walshe синтезировал из пенициллина препарат D-пеницилламин, обладающий медьвыводящим действием. Он представляет собой тиоловый препарат, содержащий сульфгидрильные группы, образующие комплексы с медь
Альтернативным методом является применение препаратов цинка (сульфат цинка, ацетат цинка). Цинк обладает минимальной токсичностью, связываясь с металлотионином кишечника, способствует экскреции меди с желчью и выведению ее с калом (а не с мочой, как при лечении тиоловыми препаратами).
Большое значение на всех стадиях болезни имеет диетотерапия, заключающаяся в ограничении продуктов с высоким содержанием меди – бобовые, баранина, куриное мясо, колбаса, рыба, шампиньоны, шоколад, кофе, орехи, редис, лук-порей и др.
При фульминантном (быстро развивающемся) гепатите прогноз крайне неблагоприятен. Патология приобретает стремительно прогрессирующее течение и обычно завершается летальным исходом. Единственно эффективным способом лечения таких больных становится трансплантация печени.
Осложнения
К основным осложнениям болезни Вильсона-Коновалова можно отнести – цирроз печени, анемию, поражение почек, нейропсихические расстройства, артриты, кардиомиопатию.
Профилактика
Профилактика возможного развития болезни Вильсона-Коновалова основана на выявлении носительства «патологического» гена у будущих родителей перед принятием решения о деторождении (при планировании беременности).
Другой способ определить возможность развития болезни — уже в период беременности — пренатальная диагностика, т.е. выявление мутаций у плода путем взятия ворсин хориона (часть плаценты забирается через шейку матки или через брюшную стенку) или при проведении амниоцентеза. Последняя методика заключается в исследовании клеток плода, находящихся в околоплодной жидкости, получаемых после прокола зародышевой оболочки.
Какие вопросы следует задать врачу
Следует ли всем лица, планирующим беременность (мужчинам и женщинам) проводить расширенный генетический тест на возможные наследственные заболевания?
Советы пациенту
Проведение генетического консультирования перед вступлением в брак – это нормальная практика во всех развитых странах.
Источник https://clinic-a-plus.ru/articles/gastroenterologiya/21502-bolezn-vilsona-konovalova.html
Источник https://www.krasotaimedicina.ru/diseases/zabolevanija_neurology/wilsons
Источник https://medaboutme.ru/zdorove/spravochnik/bolezni/bolezn_vilsona_konovalova/