Сепсис в педиатрии: алгоритмы диагностики молчаливого убийцы

Сепсис (или заражение крови) – это одно из самых проблемных состояний современного здравоохранения. До 88% случаев от этого заболевания предотвратить очень сложно и даже практически невозможно. К сожалению, сепсис – не редкость и в педиатрической практике: от него погибают даже самые маленькие, которых особенно хочется защитить. По данным Sepsis Alliance, более 75000 детей ежегодно заболевают сепсисом в Соединенных Штатах. Семь тысяч из них умирают.
«Многие жизни можно спасти, повысив осведомленность родителей и врачей о симптомах и методах диагностики сепсиса», – отмечает Ниранджан Киссун, вице-председатель Глобального альянса по проблемам сепсиса. MedAboutMe рассказывает о причинах, первых признаках и алгоритме поиска «молчаливого убийцы».

Суперфуды в косметике: сочные коктейли для здоровья кожи и волос
Причины развития сепсиса
Заражение крови – это результат проникновения в системный кровоток болезнетворных микроорганизмов. Развитию сепсиса способствуют недоношенность, иммунный дефицит, недостаточная сформированность защитных механизмов, врожденные и генетические заболевания, родовые травмы.

Первое место среди возбудителей заболевания занимают грамположительные бактерии – стафилококк, стрептококк.
Реже встречаются синегнойная и кишечная палочка, грибковая микрофлора (например, кандида).
Входные ворота для инфекции – пупочная рана, поврежденные слизистые оболочки или кожа, пищеварительный тракт или мочеполовая система. При сепсисе всегда обнаруживается первичный очаг – это может быть конъюнктивит, гнойничковые заболевания кожи, воспаление среднего уха, бронхов, глотки.
Существуют и факторы со стороны матери, которые способствуют развитию инфекции: бактериальный вагиноз, эндометрит, воспаление шейки матки, венерические заболевания. При прохождении через родовые пути микрофлора переносится в организм ребёнка, что может послужить толчком для патологического процесса.
Первые признаки: на что обратить внимание
Сепсис не зря называют «молчаливым убийцей»: его ранние симптомы могут быть настолько неспецифичны, что на них мало кто обращает внимание. Предвестниками опасного состояния могут быть вялость, слабость или беспокойство малыша, изменения аппетита, недостаточная прибавка массы тела.

Среди внешних признаков нужно обращать внимание на состояние кожи.
- Серо-желтый цвет покровов, снижение тургора – эластичности и наполненности, появление различных высыпаний.
- Иногда на коже возникают мелкие точечные кровоизлияния – признак, свидетельствующий о нарушении работы свертывающей системы крови.
- Гнойнички на теле и лице, зелено-желтое отделяемое из пупочной ранки – симптомы, которые нельзя игнорировать.
Из-за токсического поражения внутренних органов развивается спленомегалия – увеличение печени и селезенки, нарушается сердечный и дыхательный ритм, страдают надпочечники и мочевыделительная система. Часто сепсис осложняется воспалением легких – пневмонией, менингитом или остеомиелитом.
Существует еще и молниеносная форма болезни, которая считается одной из самых тяжелых. Состояние ребёнка резко ухудшается, снижается температура тела, развивается отек легких и острая почечная недостаточность: летальный исход наступает в течение нескольких суток.
Диагностический алгоритм

Дифференцировать сепсис нужно от локализованных гнойных заболеваний: пневмонии, менингита, цитомегаловирусной или герпетической инфекции, кандидоза и многих других. Диагноз может быть заподозрен педиатром во время осмотра и клинического обследования. Для этого оценивается несколько важных параметров:
- частота сердечных сокращений выше или значительно ниже возрастной нормы;
- температура тела ниже 36 или выше 38,5 градусов по Цельсию;
- увеличение частоты дыхательных движений в несколько раз по сравнению с возрастной нормой;
- повышение или снижение количества белых кровяных клеток – лейкоцитов;
- наличие дыхательной недостаточности (изменение газового состава – снижение кислорода и повышение уровня углекислого газа);
- изменение сознания по шкале комы Глазго
- падение числа тромбоцитов в общем анализе крови;
- развитие синдрома диссеминированного внутрисосудистого свертывания;
- повышение уровня печеночных ферментов в 2 раза по сравнению с нормой;
- увеличение количества С-реактивного белка.

Крайне важно обнаружение очага первичной инфекции. Если его не ликвидировать, системные воспалительные реакции будут прогрессировать, несмотря на терапию.
Именно поэтому ребёнку проводится полное обследование, а также показаны консультации большинства узких специалистов. Для обнаружения возбудителя инфекции и подбора эмпирической терапии требуется бакпосев биологических жидкостей.
Прогнозы и меры профилактики
Сепсис – тяжелое состояние с неоднозначным прогнозом. По данным разных экспертов, летальность составляет от 20-45% до 65% среди глубоко недоношенных малышей. У выздоровевших также могут отмечаться проблемы со здоровьем: склонность к респираторно-вирусным заболеваниям, задержка в физическом или умственном развитии.
Профилактика сепсиса новорожденных состоит из нескольких этапов.
- Первый – раннее выявление заболеваний мочеполовой системы у беременной женщины, а также их адекватная терапия. Для этого будущей маме необходимо проходить все осмотры и следить за своим здоровьем.
- Второй этап – осуществление противоэпидемических мероприятий в роддомах. Обязательно проводится обследование персонала на носительство патогенной микрофлоры, уборка, обработка и дезинфекция помещений и предметов.
- Третий этап – правильный уход за новорожденным, обработка кожи, глаз, ушей и пупочной ранки в соответствии с рекомендациями педиатра.

В 2020 г. специалисты медицинской школы Университета Вашингтона выяснили, что грудное вскармливание уменьшает риск развития сепсиса даже у недоношенных малышей.
Эксперты пришли к выводу, что материнское молоко содержит специальный белок – он активирует рецепторы клеток кишечного эпителия. Таким образом обеспечивается защита от проникновения болезнетворных бактерий в кровоток.
Наиболее полезно грудное молоко в первые дни лактации: оно содержит максимальное количество белка. Так можно защитить даже здоровых малышей от «знакомства» с потенциально опасной флорой.
Читайте далее

Что нужно коже малышей: гид по выбору детской уходовой косметики

Дом — место отдыха, красота, уют
Как создать уютный дом? Главное — вложить много денег? Вовсе нет. Есть секретные приемы, которые обойдутся недорого, при этом дадут большой эффект.
Лейкозы у детей: симптомы, диагностика, лечение
Лейкозы относятся к большой группе злокачественных новообразований системы крови под названием «гемобластозы». Лейкоз (от греческого слова «leukos» — белый) — злокачественная опухоль, возникающая из ранних незрелых кроветворных клеток костного мозга и метастазирующая из костного мозга в кровь, лимфатические узлы, печень, селезенку, головной мозг, спинной мозг и другие органы и ткани.
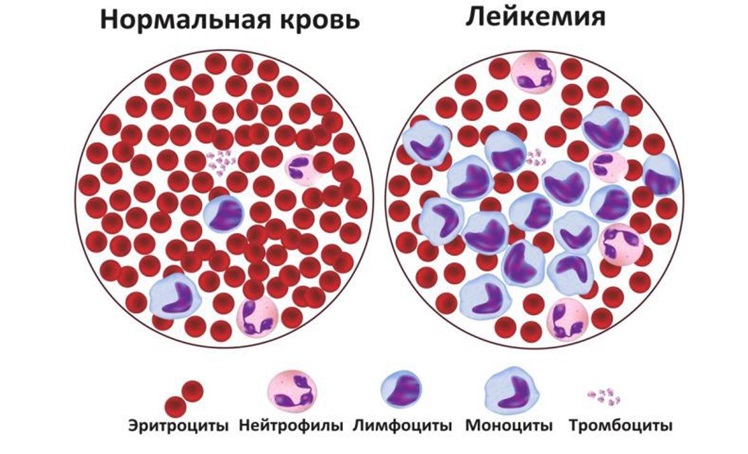
Все лейкозы можно разделить на острые лимфобластые, острые миелоидные лейкозы (ОМЛ) и хронический миелолейкоз.
Острый лимфобластный лейкоз
Более 80% всех лейкозов у детей составляет острый лимфобластный лейкоз (ОЛЛ). Причиной его развития является химерный ген TEL/AML, формирование которого происходит внутриутробно, возможно, в результате спонтанных ошибок в процессе репликации и репарации ДНК. Накопление генетических аномалий в опухолевом клоне ведет к блоку нормальной клеточной дифференцировки и нарушениям в процессе пролиферации и апоптоза.
В соответствии с франко-американо-британской (FAB) классификацией выделяют три морфологических варианта: L1, L2, L3.
Клинические симптомы ОЛЛ обусловлены степенью инфильтрации костного мозга лимфобластами, а также наличием экстрамедуллярного распространения процесса. Нередко отмечаются общие симптомы опухолевой интоксикации, а именно, повышение температуры тела, снижение аппетита, слабость, вялость. В течение процесса выделяют несколько периодов: начальный, развернутый, период ремиссии.
Развернутый период характеризуется бурным началом, многообразием клинических симптомов. К симптомам общей интоксикации присоединяются костные боли вследствие лейкозной инфильтрацией костной ткани (чаще поражаются диафизы длинных трубчатых костей), артралгии, вызванные лейкемической инфильтрацией суставов. Кожные покровы и слизистые становятся бледными. К сожалению, нередко на них появляются кровоизлияния, обусловленные геморрагическим синдромом, а также кровотечения (носовые, желудочно-кишечные, почечные). Увеличение периферических лимфатических узлов (шейно-надключичных, подмышечных, паховых) является одним из основных симптомов заболевания. Практически у всех пациентов отмечается обусловленное пролиферацией лейкозных клеток увеличение печени и селезенки. В некоторых случаях у пациентов поражение кожи и слизистых оболочек проявляется в виде лейкемидов, некроза, гингивита и стоматита.
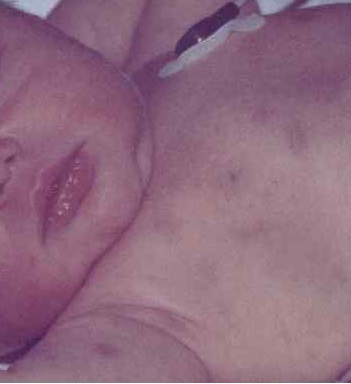
Таким образом, можно выделить несколько симптомокомплексов, характерных для ОЛЛ:
- гиперпластический – лимфоаденопатия, боли в костях, тяжесть и боли в левом и правом подреберьях, гепатоспленомегалия;
- анемический – головокружение, мерцание мушек перед глазами, одышка при физической нагрузке, сердцебиение, шум в голове и ушах;
- геморрагический – кожные геморрагии, кровоточивость десен, носовые кровотечения;
- интоксикационный – повышение температуры тела, слабость, отсутствие аппетита, оссалгии;
- синдром инфекционных осложнений – присоединение тяжелых пневмоний.
При диагностике оцениваются морфологические особенности бластов костного мозга и периферической крови. Помимо обнаружения опухолевых клеток лимфоидной линии кроветворения при окраске по Романовскому – Гимзе, проводятся следующие методы исследования:
- цитохимические – позволяют отнести бласты к лимфоидному или миелоидному ростку (тест на миелопероксидазу, фосфолипиды, гликоген), отдельным клеточным линиям;
- иммунофенотипические – определяют иммунные маркеры клеток (CD);
- цитогенетические – определяют аномалии кариотипа и хромосомные аберрации (делеции, транслокации, инверсии и др.);
- молекулярно-биологические – позволяют установить количество клеток с определенной аберрацией во всей массе костного мозга.
Для подтверждения диагноза ОЛЛ необходимо комплексное обследование, в котором ведущая роль отводится морфологическому методу.
В настоящее время используются программы лечения BFM (БФМ: Берлин-Франкфурт-Мюнстер) и МВ (МБ: Москва-Берлин).
Все лечение можно разделить на базисное и сопроводительное. Базисная терапия представляет собой системную и локальную химиотерапию и, при необходимости, лучевую терапию. Сопроводительное лечение обязательно назначается для профилактики инфекционных осложнений и коррекции постцитостатических реакций. Выделяют следующие этапы в лечении злокачественных процессов: индукция ремиссии, консолидация ремиссии (как правило, несколько фаз), поддерживающее лечение.
Острый миелоидный лейкоз
Острый миелоидный лейкоз составляет 15% всех острых лейкозов у детей. Существующая FAB-классификация (Франко-Американо-Британская) позволяет разделить ОМЛ на следующие варианты:
- M0 (минимально дифференцированный ОМЛ), который характеризуется бластными клетками средних размеров с округлым ядром, отсутствием зернистости и палочек Ауэра в цитоплазме;
- М1 (ОМЛ без созревания), при котором менее 90% неэритроидных клеток представлены бластными клетками с преобладающей мезогенераций с округлыми ядрами и высоким ядерно-цитоплазматическим отношением;
- М2 (ОМЛ с созреванием), характеризующийся бластными клетками средних размеров с высоким и умеренным ядерно-цитоплазматическим отношением (20 – 90% всех неэритроидных клеток), в их цитоплазме выражено наличие азурофильной зернистости и палочек Ауэра;
- М2 баз (базально-клеточный), бластные клетки характеризуются наличием базофильной зернистости, составляет не более 0,5% острых нелимфобластных лейкозов;
- М3 (промиелоцитарный) вариант характеризуется бластными клетками крупных размеров с ядрами неправильной формы, отмечается крупная зернистость и палочки Ауэра в цитоплазме;
- М3v (гипогранулярный) с отсутствием зернистости;
- М4 (миеломонобластный): бластные клетки с ядрами округлой и неправильной формы, низким и умеренным ядерно-цитоплазматическим отношением, некоторые бластные клетки могут содержать зернистость, палочки Ауэра;
- М5а (монобластный без созревания), при котором монобласты составляют свыше 80% моноцитоидных клеток, бластные клетки крупных размеров с ядрами бобовидной или лопастной формы, в части из них просматривается зернистость, палочки Ауэра при этом не выявляются;
- М5b (монобластный с созреванием): монобласты составляют менее 80% моноцитоидных клеток, крупные с ядрами моноцитоидной формы, цитоплазмой без зернистости, палочки Ауэра не выявляются;
- М6 (эритромиелоз): более 50% бластом в костном мозге представлены эритробластами;
- М7 (мегакариобластный) лейкоз, при котором бластные клетки полиморфны, с отростчатой базофильной цитоплазмой, какие-либо специфические морфоцитохимические признаки отсутствуют.
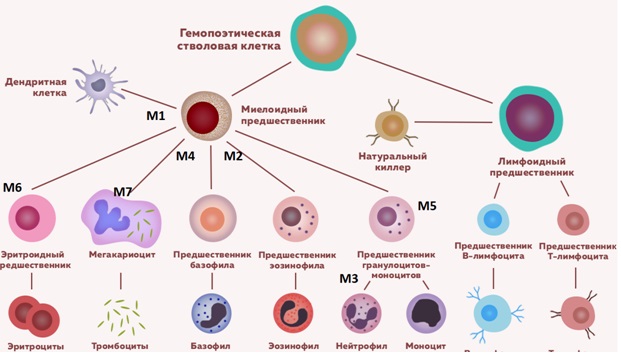
Схема гемопоэза с клетками предшественниками острого миелоидного лейкоза
Клиническая картина ОМЛ также складывается из анемического, геморрагического и токсического синдромов, которые являются следствием снижения продукции эритроцитов, тромбоцитов и гранулоцитов.
У 50% пациентов отмечается увеличение размеров печени (гепатомегалия) и селезенки (спленомегалия) вследствие инфильтрации органов опухолевыми клетками.
Внекостномозговые проявления заболевания связаны с лейкозной инфильтрацией центральной нервной системы и метастатическим поражением оболочек и вещества головного и спинного мозга (нейролейкемия). В этих ситуациях отмечается постоянная головная боль, возможна рвота, вялость, выявляется отек дисков зрительных нервов, могут быть нистагм, косоглазие, другие признаки поражения черепно-мозговых нервов, выявляются ригидность затылочных мышц, симптом Кернига.
Решающую роль в диагностике также имеет цитохимическое, иммунофенотипическое и морфологическое исследование бластов в костном мозге и периферической крови.
Ремиссию заболевания можно достичь посредством проведения высокодозной полихимиотерапии с последующей трансплантацией гемопоэтических стволовых клеток от HLA-геноидентичного родственного или альтернативного (неродственного, гаплоидентичного) донора у пациентов группы высокого риска рецидива. Благодаря адаптивным протоколам удается достичь ремиссии у 90% детей.
Хронические миелолейкоз
Хронический лейкоз – это вариант гемобластоза, субстратом которого являются созревающие клетки. У детей встречается только хронический миелолейкоз, который характеризуется пролиферацией гранулоцитарного ростка, гиперплазией миелоидной ткани, миелоидной метаплазией кроветворных органов, ассоциированной с хромосомной транслокацией t(9;22)(q34;q11), в результате которой образуется химерный онкоген BCR-ABL.
В течение хронического миелолейкоза выделяют три фазы:
- Хроническая фаза: выраженные симптомы отсутствуют.
- Фаза акселерации: повышение уровня лейкоцитов (>50 х 10 9 /л), бластов в периферической крови и костном мозге (> 10%); анемия и тромбоцитопения; персистирующий тромбоцитоз (> 1000 х 10 9 /л).
- Острая (бластная) фаза: миелобласты >30% в крови или в костном мозге; лимфобласты >30% в крови или в костном мозге; наличие бластных клеток в ликворе.
В дебюте заболевание трудно диагностировать, поскольку основные симптомы обусловлены общим опухолевым симптомокомплексом и носят преходящий характер. Наиболее частые симптомы, присоединяющиеся позднее – гепатомегалия и спленомегалия. Нарастающая интоксикация приводит к появлению слабости, утомляемости, повышению температуры тела, болям в костях.
В периферической крови отмечается гиперлейкоцитоз (до 200 – 300 х 10 9 /л и более) с увеличением содержания гранулоцитов до 95% и преобладанием незрелых клеток гранулоцитарного ряда: промиелоцитов, миелоцитов, метамиелоцитов, миелобластов, базофилов (до 10%) и эозинофилов (до 5%). Характерна анемия и повышение СОЭ. Уровень тромбоцитов преимущественно в норме, однако может отмечаться гипертромбоцитоз (до 600 х 10 9 /л и более).
В пунктате костного мозга отмечается увеличение числа миелокариоцитов за счет пролиферирующего пула клеток гранулоцитарного ряда с увеличением базофилов и эозинофилов. Позднее отмечается угнетение эритронормобластического и мегакариоцитарного ростков кроветворения.
Основным средством терапии и стандартом лечения хронического миелолейкоза в настоящее время является применение ингибиторов тирозинкиназы (ИТК). Данные препараты имеют механизм таргетного (целенаправленного) воздействия на BCR-ABL-положительные опухолевые клетки и должны назначаться всем пациентам после подтверждения диагноза. Для оценки эффективности и переносимости терапии ИТК рекомендуется регулярный мониторинг гематологических, цитогенетических и молекулярно-генетических и других показателей у пациента.
Список литературы
- Кузник Б. И. Клиническая гематология детского возраста: учеб. пособие / Б. И. Кузник, О. Г. Максимова. — М.: Вузовская книга, 2010. — 496 с.
- Румянцев А. Г. Практическое руководство по детским болезням. Т. 4. Гематология/онкология детского возраста / А. Г. Румянцев, Е. В. Самочатова. — М. : Медпрактика-М, 2004. — 792 c.
- Румянцев А.Г. Эволюция лечения острого лимфобластного лейкоза у детей. Педиатрия, 2016; 95(4): 11-22.
- Möricke A., Zimmermann M., Reiter A., et al. Long-term results of five consecutive trials in childhood acute lymphoblastic leukemia performed by the ALL-BFM study group from 1981 to 2000. Leukemia. 2010 Feb;24(2):265-84. doi: 10.1038/leu.2009.257.
- Creutzig U, van den Heuvel-Eibrink MM, Gibson B, et al. AML Committee of the International BFM Study Group. Diagnosis and management of acute myeloid leukemia in children and adolescents: recommendations from an international expert panel. Blood. 2012 Oct 18;120(16):3187-205. doi: 10.1182/blood-2012-03-362608.
- de la Fuente J, Baruchel A, Biondi A, de Bont E, Dresse MF, Suttorp M, Millot F; International BFM Group (iBFM) Study Group Chronic Myeloid Leukaemia Committee. Managing children with chronic myeloid leukaemia (CML): recommendations for the management of CML in children and young people up to the age of 18 years. Br J Haematol. 2014 Oct;167(1):33-47. doi: 10.1111/bjh.12977.

Авторская публикация:
Кулева С.А.
Заведующая отделением, врач-детский онколог, ведущий научный сотрудник, профессор НМИЦ онкологии им. Н.Н. Петрова

Иванова Светлана Вячеславовна
Врач-детский онколог, научный сотрудник, кандидат наук НМИЦ онкологии им Н.Н. Петрова
Что вам необходимо сделать
Если вы хотите узнать побольше о бесплатных возможностях ФБГУ НМИЦ онкологии им. Н.Н. Петрова Минздрава России, получить очную или заочную консультацию по диагностике и лечению, записаться на приём, ознакомьтесь с информацией на официальном сайте.
Если вы хотите общаться с нами через социальные сети, обратите внимание на аккаунты в ВКонтакте и Одноклассники.
Первые симптомы лейкоза у детей
Онкологические заболевания, по праву считающиеся чумой 21 века, не щадят даже детей. По статистике среди детской онкологии лидирующую позицию занимает лейкемия — патология клеток крови. Она приходится на 35% случаев и чаще диагностируется у мальчиков. Важно вовремя распознать лейкоз, симптомы у детей, обнаруженные на ранней стадии, не приведут к серьезным осложнениям. Рассмотрим подробнее, что представляет собой страшная патология, чтобы своевременно принять меры и спасти жизнь ребенка.
Лейкоз — что это
Лейкоз, или лейкемия, белокровие, — это опухолевая патология злокачественного характера, поражающая кроветворную и лимфатическую ткани. Лейкемия у детей характеризуется изменением кровотока костного мозга, сопровождающегося замещением здоровых кровяных клеток незрелыми бластами лейкоцитарного ряда.

Количество детей, страдающих от лейкоза, неуклонно растет. Высока детская смертность от рака крови.
Для лейкемии у ребенка характерно не поддающееся контролю скопление в костном мозге белых патологических кровяных клеток.
Выделяют две формы лейкоза:
- Острая, характеризующаяся отсутствием образования красных кровяных клеток и выработкой большого количества белых незрелых клеток.
- Хроническая форма сопровождается длительным замещением здоровых клеток патологическими белыми бластами. Характеризуется более щадящим течением. По статистике пациенты с диагнозом «хронический лейкоз крови» живут от 1 года и более.
Для лейкемии нехарактерно перетекание форм.
Различают лимфообластную и нелимфообластную разновидности острого лейкоза.
Лимфообластной лейкоз формируется из лимфобластов, располагающихся в красном костном мозге, в последующем распространяющихся на лимфоузлы, селезенку.
Диагностируется у детей, достигших 1 года.
Нелимфообластной лейкоз, или миелоидный, характеризуется образованием опухоли миелоидного кровяного отростка, сопровождающейся очень быстрым размножением белых клеток крови. Данный вид патологии диагностируется реже. В группе риска находятся мальчики и девочки двух-трехлетнего возраста.
Почему появляется злокачественная патология
Ученым так и неясны некоторые причины возникновения лейкоза у детей. Однако существуют некоторые теоретико-практические обоснования ответа на вопрос, почему дети болеют лейкозом. Выделяют следующие причины лейкоза у детей:
- Генетическая предрасположенность. Формируются патологические гены в результате внутриутробных хромосомных изменений, производящих при этом вещества, препятствующие созреванию здоровых клеток.
- Вирусное инфицирование организма. В результате перенесенных ребенком болезней вирусной этиологии, например, ветряная оспа, мононуклеоз, ОРВИ и др., вирусы встраиваются в клеточный геном.
- Иммунодефицит. Иммунная система не справляется с уничтожением чужеродных организмов и перестает уничтожать собственные патологические клетки, включая злокачественные.
- Радиационное излучение приводит к мутации кровяных клеток. К факторам риска относится облучение матери (рентген, томография) в период вынашивания плода, а также проживание в радиоактивной зоне.
- Пагубные привычки родителей, особенно матери. Курение, употребление алкоголя и наркотическая зависимость.
- Вторичный лейкоз после перенесенной лучевой или химиотерапии при другом онкозаболевании.
Развивается также лейкоз у детей по причине образования озоновых дыр в результате активного солнечного излучения. Причины лейкемии у детей кроются также в генетических патологиях, таких как синдромы Дауна, Блума и др., а также полицитемия.
Как распознать патологию
Обычно первые признаки лейкоза заявляют о себе постепенно и сопровождаются симптомами, свойственными другим патологиям:
- повышенная утомляемость;
- отсутствие аппетита;
- расстройство сна;
- беспричинное повышение температуры;
- костная и суставная боль.
Как видите, указанные признаки лейкоза у детей похожи на симптомы обычной простуды. Часто они сопровождаются появлением по всему телу красных пятен, а также увеличением печени и селезенки.
Это требует незамедлительного обращения за медицинской помощью.
Встречаются случаи детского лейкоза, для симптомов которого характерно внезапное проявление выраженного отравления организма (тошнота, рвота, слабость) или кровотечения, чаще всего носовые.
Симптомы лейкемии у детей зависят от особенностей развития злокачественного недуга. Патологические клетки, поражая организм, продолжают активное размножение, приводя к острой форме лейкемии.
Для нее характерны следующие симптомы лейкоза у детей:
- Резкое падение гемоглобина. Развивается анемия, сопровождающаяся вялостью, мышечными болями, быстрой усталостью.
- Снижение уровня тромбоцитов провоцирует развитие геморрагического синдрома, проявляющегося различными кровоизлияниями, кровотечениями из носа, десен, желудка, кишечника, легких. Даже царапина становится источником активного излияния крови у детей.
- Синдром иммунодефицита проявляется в результате повышенной концентрации лейкоцитов в крови, что делает организм ребенка уязвимым к инфекционно-воспалительным процессам. Нередко возникают гингивиты, стоматиты, тонзиллиты и другие инфекции. Очень часто дети, больные лейкозом, умирают вследствие развития тяжелых форм пневмонии или сепсиса.
- Интоксикация организма проявляется при детском лейкозе лихорадочным состоянием, анорекисей, рвотой, приводит развитию гипотрофии. Опасно осложнением лейкемической инфильтрации головного мозга.
- Сердечно-сосудистые расстройства с признаками тахикардии, аритмии, изменениями сердечной мышцы.
- Ярко выраженная бледность или желтушность слизистых и эпидермиса.
- Болезненное увеличение лимфоузлов.
- При поражении головного мозга при лейкозе у детей фиксируется головокружение, мигренеподобные боли, парез конечностей.
Лейкоз у новорожденных распознается по явному отставанию в развитии.
Различают три стадии лейкоза, по симптомам у детей они обнаруживают себя таким образом:
- Начальная стадия выражается незначительным ухудшением здоровья (ранние признаки описаны выше).
- Развернутая стадия протекает на фоне ярко выраженных симптомов, перечисленных ранее. Все признаки лейкемии говорят о необходимости полного обследования организма для исключения серьезных заболеваний.
- Терминальная стадия не вылечивается. Сопровождается полным выпадением волос, сильным болевым синдромом, образованием метастазов, приводящим к активному распространению патологических клеток и лейкозному поражению всего организма.
Не допустить появления необратимых последствий поможет обращение к врачу, ранняя диагностика рака крови, строгое исполнение всех врачебных назначений.
Диагностика лейкоза
Главная ответственность в распознавании первичных проявлений белокровия лежит на педиатре, далее ребенком занимается онкогематолог.
Детский лейкоз распознается с помощью следующих лабораторных исследований:
- клинический анализ крови;
- стренальная пункция и миелограмма — обязательные методики в диагностике лейкоза;
- трепанобиопсия;
- цитохимические, цитогенетические и иммунологические исследования;
- УЗИ внутренних органов, а также лимфоузлов, слюнных желез, мошонки;
- рентгенография;
- компьютерная томография.
Кроме того, требуется обязательное консультирование у невролога и офтальмолога.
Лечение тяжелого недуга
На самый частый вопрос, лечится ли лейкоз у детей, к сожалению, однозначно ответить нельзя. Статистика оперирует следующими фактами: 10-20% детей вылечиться не удается. Однако врачи утверждают, что лейкозы у детей — не приговор, и 80-90% детей вылечиваются благодаря ранней диагностике и возможностям современной медицины.
Главная цель в лечении рака крови — уничтожение всех незрелых бластных клеток лейкоцитарного ряда путем применения комплексной терапии.
Лечение лейкоза у детей осуществляется строго в стационаре под постоянным наблюдением медицинского персонала. Поскольку организм ребенка подвержен быстрому инфицированию, ему выделяют отдельную палату, исключают внешние контакты, требуют ношения повязки, защищающей дыхательные органы.
При лейкозе у детей, для лечения которого требуется много времени и сил, важно набраться терпения родителям и во всем поддерживать ребенка для достижения стойкой ремиссии недуга.
Основным терапевтическим методом при лейкемии является полихимиотерапия, проводимая при строгом соблюдении правил, сроков и дозы препаратов. Главная задача врача — подобрать точную дозировку лекарств, чтобы уничтожить патологические клетки и не навредить здоровью маленького пациента. Часто процесс лечения сопровождается очень тяжелым состоянием больного.
В дополнение к химиотерапевтическому лечению лейкоза лечащий врач назначает иммунотерапию, включающую введение вакцин БЦЖ, оспы, лейкозных клеток.
В отдельных случаях прибегают к пересадке костного мозга, стволовых клеток.
Исходя из того, какие проявляются у детей симптомы, лечение лейкемии может варьироваться.
В целом терапия, устраняющая симптомы болезни, включает следующие процедуры:
- переливание крови;
- назначение кровоостанавливающих препаратов при геморрагическом синдроме;
- антибиотики для лечения инфекций, часто сопровождающих лейкоз;
- дезинтоксация путем проведения плазмафереза, гемосрбции.
Терапия детского лейкоза поддерживается правильным сбалансированным питанием:
- отказом от жирной, острой, маринованной продукции;
- ограничением употребления полуфабрикатов;
- употреблением свежей, только что приготовленной пищи в теплом жидком виде;
- полным исключением пробиотиков.
Можно ли предотвратить повторное развитие лейкемии? Врачи отвечают положительно, если строго следовать врачебным рекомендациям и вести здоровый образ жизни.
Каковы прогнозы болезни
Отсутствие лечения рака крови у детей приводит к летальному исходу. При раннем распознавании лейкоз излечим в 80% случаях. Чаще всего благоприятный исход наблюдается при отсутствии рецидивов после химиотерапии в течение 5 лет.
Если болезнь не заявляла о себе около 7 лет, возможно полное избавление от страшного недуга.
Менее благоприятный исход у хронической формы миелоидного лейкоза, а также при развитии лейкемии у новорождённого (до 1 года) ребенка.
Однако эти данные условны, полный рецидив может возникнуть и при острой лейкемии. Что влияет на прогноз и течение болезни, точно утверждать сложно. Это зависит от каждого конкретного случая.
Главное помните, что при первых симптомах белокровия у детей следует немедленно обратиться в медицинское учреждение. Жизнь маленького пациента зависит от ваших действий и грамотного лечения, назначенного врачом.
Источник https://medaboutme.ru/articles/sepsis_v_pediatrii_algoritmy_diagnostiki_molchalivogo_ubiytsy/
Источник https://nii-onco.ru/rak-u-detej/lejkozy-u-detej-simptomy-diagnostika-lechenie/
Источник https://clinic-a-plus.ru/articles/pediatriya/2488-leykoz-simptomy-u-detey-priznaki-kak-proyavlyaetsya.html

