Мужское аутоиммунное бесплодие
Результаты анализов 3660 образцов эякулята, комплексное клинико-лабораторное обследование 1066 мужчин из бесплодных пар и 37 фертильных позволяют сделать вывод, что наличие аутоиммунных реакций против сперматозоидов всегда приводит к снижению вероятности наступления беременности. Нарушения качества спермы и реальной фертильности нарастают с увеличением доли прогрессивно-подвижных сперматозоидов, покрытых антиспермальными антителами (АСАТ). Доля первичных нарушений и продолжительность бесплодия по сравнению с фертильными мужчинами статистически достоверны при любых значениях MAR%IgG>0%. По сравнению с бесплодными без АСАТ, при нормозооспермии вероятность наступления беременности у АСАТ-позитивных мужчин существенно снижена при MAR% IgG>50%. Частота наступления беременности в естественном цикле без лечения от мужчин с MAR%IgG>50% составляет менее 2%, а при MAR%IgG=100% практически равна 0. Выявлена негативная корреляция между долей всех живых сперматозоидов, покрытых АСАТ классов IgG, IgA, IgM и количественными показателями спермограммы, но не с продолжительностью бесплодия. Лечение бесплодных мужчин с аутоиммунными реакциями против сперматозоидов требует использования специальных методов лечения (корикостероиды, протеолитические ферменты) независимо от величины MAR%IgG>0%. Неспецифическая стимуляция сперматогенеза у мужчин с АСАТ не приводит к улучшению количественных показателей спермограммы за счет усиления аутоиммунного процесса.
Введение
Известно [1-3 и др.], что развитие аутоиммунных реакций против сперматозоидов обычно приводит к бесплодию. Признаком таких реакций служит присутствие в сперме антиспермальных антител (АСАТ), а стандартными измеряемыми показателями — доля сперматозоидов, покрытых АСАТ [4-6]. Однако АСАТ могут встречаться и у мужчин с подтвержденной фертильностью [7-9], поэтому до сих пор не ясно, какое количество АСАТ является нормальным, а какое — патологическим, приводящим к нарушению репродуктивной функции. За последние 20 лет эксперты ВОЗ трижды меняли границу нормы. Согласно первой редакции «Руководства ВОЗ по лабораторному исследованию спермы человека и взаимодействия спермы с цервикальной слизью» (1980) диагноз «иммунологическая причина (первопричина) мужского бесплодия» нужно было ставить, когда не менее 40% подвижных сперматозоидов были покрыты АСАТ. Вторая и третья редакция Руководства (1987,1992) рекомендовали ставить такой диагноз при более чем 10% АСАТ-позитивных сперматозоидах, последняя четвертая (1999) — когда таких сперматозоидов не менее половины. В то же время, как отмечают сами эксперты [10], некоторые клиники вообще не учитывают этот фактор, не считая его клинически значимым, другие по-прежнему опираются на непрямые тесты агглютинации и иммобилизации, во многих центрах предлагают свои диагностические критерии «иммунологического бесплодия», противоречащие друг другу.
Объективными препятствиями для установления границ нормы для эякулята, в т.ч. присутствия АСАТ, являются несколько факторов. Во-первых, большая индивидуальная и популяционная изменчивость показателей спермограммы у бесплодных и фертильных мужчин, в результате чего распределение переменных не имеет отчетливых разрывов или двух различных пиков, из которых один соответствовал бы «норме», другой — «патологии» [11]. Во-вторых, систематические ошибки, связанные с субъективной оценкой количества АСАТ-позитивных сперматозоидов исследователем при микроскопии в случае применения рекомендованных ВОЗ MAR- и IBT-тестов [5]. В-третьих, влияние на вероятность наступления беременности дополнительных (случайных) факторов, в частности патологии репродуктивных органов у супруги или наличие у нее фертильных сексуальных партнеров вне брака. В результате, диагноз, прогноз и ожидаемые результаты лечения для конкретного больного не могут быть определены однозначно, а могут быть выражены только через вероятность.
С целью получить собственные данные, характеризующие зависимость между количеством АСАТ у мужчин и вероятностью нарушения репродуктивной функции супружеской пары выполнено настоящее исследование.
Для подтверждения роли аутологичных АСАТ как фактора бесплодия использованы три стандартных критерия, рекомендованные для оценки состояния как патологического [12]: 1) необычность состояния с точки зрения статистики; 2) проявление состояния в виде болезни, т.е. связь состояния с нарушением функции; 3) возможность улучшения состояния при лечении.
Материалы и методы
Был проведен анализ образцов эякулята 3660 мужчин, обследованных по поводу бесплодия, воспалительных заболеваний репродуктивного тракта и профилактически. Комплексный анализ эякулята выполняли в соответствии с критериями ВОЗ (1992).
Были проанализированы данные комплексного клинико-лабораторного обследования 480 бесплодных мужчин с диагностированными АСАТ. Группу сравнения составили 36 фертильных и 550 бесплодных мужчин без АСАТ. Методом MAR [13] определяли долю подвижных сперматозоидов, покрытых антителами IgG и IgA, методом ИФА (ELISA) — концентрацию АСАТ в сыворотке крови [14], методом проточной цитофлуорометрии (ПЦМ) — процент спермиев, покрытых антителами классов IgG, IgA, IgM, количество антител на один сперматозоид, а так же спонтанную и индуцированную ионофором А23187 акросомальную реакцию [15]. Выполняли исследования гонадотропинов ЛГ, ФСГ, ПРЛ, тестостерона (Т), эстрадиола (Е2) и секс-гормон-свяхывающего глобулина (СГСГ). Учитывалось наличие скрытых инфекций репродуктивного тракта (ИРТ); диагностику ИРТ осуществляли по наличию специфической ДНК методами ДНК-зондов и ПЦР [16], для условно-патогенных микроорганизмов — посевом на питательные среды. Мужчины с острым течением воспалительного процесса (уретрит, орхит, эпидидимит, простатит) были исключены из исследования.
Женщины из бесплодных пар находились под наблюдением гинекологов и при необходимости получали соответствующую терапию.
Полученные данные обрабатывали методами вариационной статистики при помощи t критерия Стьюдента и F критерия Фишера для независимых и парных значений и ХИ-квадрат, вычисляли коэффициент корреляции r Пирсона.
Результаты
Частота обнаружения АСАТ зависела от использованных методов. Наиболее чувствительным оказалось прямое определение антител на сперматозоидах — MAR-тест. Совпадение положительных результатов ИФА с результатами MAR%IgG>0 (т.н. чувствительность) наблюдалась в 6% случаев (2 из 32).
Имелись различия в частоте обнаружения АСАТ у мужчин, обследуемых по различным показаниям: с профилактической целью, в случаях бесплодного брака, привычного невынашивания, хроническом неспецифическом простатате, или скрининговом обследовании по поводу наступившей беременности. Наиболее высокий процент выявления АСАТ наблюдался в группе бесплодных пациентов, наименьший — при хроническом неспецифическом простатите (табл.1).
| Показатели> | Фертильные (n=36) | Бесплодные (n=1374) | Неспециф. простатит (n=155) |
|---|---|---|---|
| Иммунологический фактор (абс. число/проценты) | 8 (22,2%) | 660 (48,0%) | 8 (5,2%) |
| Средние значения MAR у пациентов с АСАТ (%) | 24,8.10,8 | 44,8.1,5 | 19,0.11,7 |
| Min и Max значения MAR у пациентов с АСАТ (%) | 1 – 60% | 2 – 100% | 1 – 100% |
| Знач. MAR меньше 10% (абс. число/проценты) | 3 (8,3%) | 132 (9,6%) | 5 (3,2%) |
| Знач. MAR10-49% (абс. число/проценты) | 3 (8,3%) | 268 (19,5%) | 2 (1,3%) |
| Знач. MAR не менее 50% (абс. число/проценты) | 2 (5,5%) | 260 (18,9%) | 1 (0,6%) |
Таблица 1. Частота выявления АСАТ методом MAR у мужчин репродуктивного возраста
В группе фертильных мужчин, жены которых забеременели без лечения в естественном цикле, АСАТ присутствовали в 22% случаев (8/36), в т.ч. MAR%IgG от 10 до 49% — у 3 человек (8%) и больше 50% — у 2 чел (5%). Максимальное значение MAR%IgG при этом составляло 60%, IgA — 10%. Зарегистрированные случаи беременности в естественном цикле без лечения (более чем 400 находящихся под наблюдением пар с АСАТ у мужчин) составляют ожидаемую вероятность зачатия: 4,2% при MAR%IgG
Анализ данных анамнеза показал (рис.1), что у всех мужчин из бесплодных пар средняя продолжительность половой жизни в браке без применения контрацепции и доля первичного нарушения репродуктивной функции существенно больше, чем у фертильных (P<0,001). У бесплодных мужчин с АСАТ по сравнению с бесплодными без АСАТ различия в доле первичных нарушений становятся статистически значимыми для MAR%IgG>80% (P<0,01-0,001), а продолжительность бесплодия - для групп с MAR%IgG 50-59% и 100%.
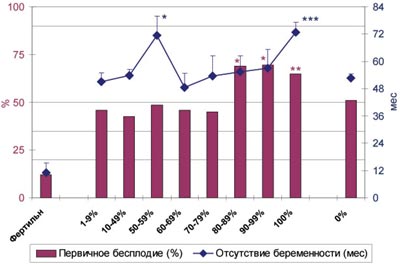
Рис. 1. Зависимость длительности и характера бесплодия от величины MAR%IgG (n=1066).
* — различия между бесплодными с АСАТ и без АСАТ достоверны с P
| Показатели | азооспермия | конц. меньше 5 млн/мл | конц. от 5 до 19 млн/мл | |||
|---|---|---|---|---|---|---|
| С АСАТ | Без АСАТ | С АСАТ | Без АСАТ | С АСАТ | Без АСАТ | |
| Человек (число) | 11 | 22 | 41 | 72 | 68 | 94 |
| Возраст (лет) | 32,8.1,41 | 33,23.0,95 | 33,2.1,11 | 30,19.1,10 | 32,29.0,84 | 30,56.0,83 |
| Яички ( %) | <18** / >0 | 5 | 40/6 | 53/0 | 20/8 | 29/2 |
| Придатки ( %) | 58 | 23 | 29/37 | 31/16 | 12/31 | 20/23 |
| Варикоцеле (%) | 33 | 33 | 38 | 34 | 31 | 31 |
| ИРТ (%) | 50 | 25 | 33 | 37 | 36 | 30 |
| Конц. (млн./мл) | 0 | 0 | 1,57.0,22 | 1,73.0,18 | 12,68.0,53 | 12,31.0,37 |
| Подв. А+В (%) | 0 | 0 | 10,8.1,27 | 10,1.1,15 | 22,54.1,14 | 22,81.0,98 |
| Морфол. (%) | 0 | 0 | 42,72.3,55 | 44,71.1,98 | 32,28.1,54 | 37,58.1,46 |
| MAR IgG непр. (%) | 45,4.10,25 | 0 | 45,41.5,93 | 0 | 39,06.6,92 | — |
| MAR IgA непр. (%) | 55,0.5,00 | — | 34,17.8,60 | — | 7,88.1,47 | — |
| ЛГ (МЕ/л) | 7,20.1,61 | 7,07.0,92 | 6,37.0,98 | 6,62.0,51 | 4,67.0,51 | 4,35.0,31 |
| ФСГ (МЕ/л) | 9,20.3,84 | 12,85.2,23 | 7,90.1,17 | 7,10.0,70 | 5,32.0,49 | 5,26.0,37 |
| Т (пМ/л) | 14,91.1,91 | 15,48.1,47 | 16,85.1,37 | 17,97.1,09 | 19,14.1,62 | 20,07.0,88 |
| СГСГ (нМ/л) | 75,63.16,50* | 38,65.6,59 | 41,86.6,23 | 54,47.3,90 | 41,34.3,71** | 56,43.3,43 |
| Т свободный (пМ/л) | 22,35.6,52 | 44,09.9,71 | 53,81.10,64 | 42,61.4,45 | 56,09.7,60 | 39,16.4,08 |
Таблица 2. Особенности строения наружных половых органов, секреторная и эндокринная функция яичек у бесплодных мужчин с олигозооспермией на фоне АСАТ и без АСАТ в зависимости от концентрации сперматозоидов в эякуляте, M m и %.
Поскольку нарушения фертильности у MAR-позитивных мужчин могут быть связаны с ухудшением количественных показателей спермограммы, а не с действием АСАТ, были выделены выборки бесплодных пациентов с нормальной концентрацией, подвижностью и морфологией сперматозоидов, отличающиеся только по наличию и отсутствию АСАТ.
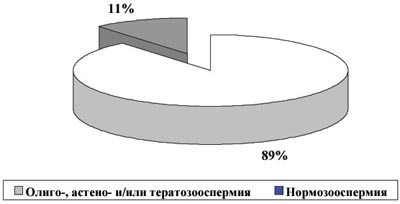
Рис. 2. Доля бесплодных пациентов с нормозооспермией без АСАТ (n=550)
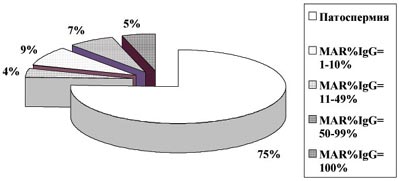
Рис. 3. Доля мужчин c нормозооспермией при иммунном факторе бесплодия (n=480)
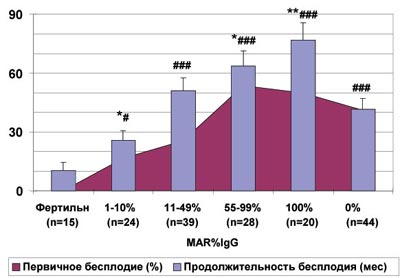
Рис. 4. Особенности нарушения репродуктивной функции у мужчин с нормозооспермией без инфекций репродуктивного тракта в зависимости от количества подвижных сперматозоидов, покрытых антиспермальными антителами (MAR%IgG).
Данные закономерности подтвердил корреляционный анализ. Показано (рис.5), что у бесплодных мужчин с нормозооспермией имеется статистически значимая зависимость продолжительности бесплодия от количества подвижных сперматозоидов, покрытых антиспермальными антителами класса IgG. То, что связь является причино-следственной, подтверждает отсутствие в этой группе бесплодных мужчин значимой корреляции продолжительности бесплодия с другими показателями спермограммы: концентрацией сперматозоидов (r=0,00), их подвижностью (r=+0,11) и морфологией (r=+0,06), концентрацией лейкоцитов (r=-0,06), спонтанной и индуцированной ионофором акросомальной реакцией (r=+0,15 и -0,19 соответственно, P>0,05). С увеличением доли сперматозоидов, покрытых АСАТ класса IgA, также увеличивается продолжительность бесплодного брака; одновременно ухудшаются количественные показатели спермограммы, оцениваемые по интегральному индексу качества спермы (ИКС) — количеству прогрессивно-подвижных и морфологически нормальных сперматозоидов в эякуляте (рис.6).
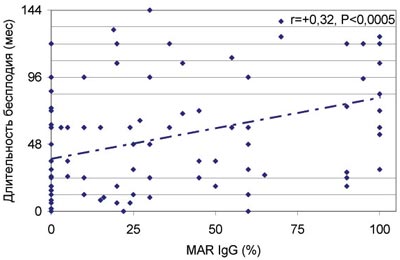
Рис. 5. Зависимость продолжительности бесплодия от количества подвижных сперматозоидов, покрытых антиспермальными антителами (MAR%IgG), при нормальной концентрации, подвижности и морфологии сперматозоидов в эякуляте (нормозооспермия) в отсутствие инфекций репродуктивного тракта.
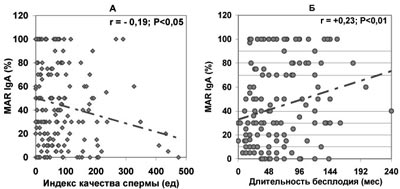
Рис. 6. Зависимость от величины MAR%IgA количества прогрессивно подвижных и морфологически нормальных сперматозоидов в эякуляте — ИКС (А) и продолжительности бесплодия при нормозооспермии (Б).
В то же время отсутствует значимая зависимость продолжительности бесплодия от доли всех живых сперматозоидов, покрытых АСАТ IgG, IgA, IgM (по данным ПЦМ), несмотря на то, что с ростом ПЦМ% наблюдается существенное ухудшение качества спермы (рис.7-9).
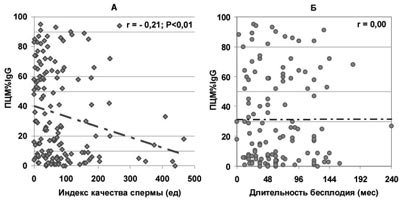
Рис. 7. Зависимость от величины ПЦМ%IgG количества прогрес-сивно-подвижных и морфологически нормальных сперматозоидов в эякуляте — ИКС (А) и продолжительности бесплодия при нормозооспермии (Б).
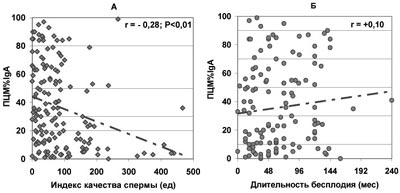
Рис. 8. Зависимость от величины ПЦМ%IgА количества прогрессивно подвижных и морфологически нормальных сперматозоидов в эякуляте — ИКС (А) и продолжительности бесплодия при нормозооспермии (Б).
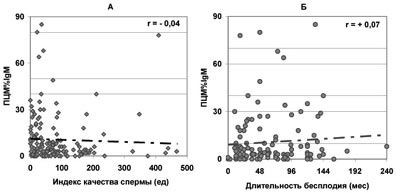
Рис. 9. Зависимость от величины ПЦМ%IgM количества прогрессивно подвижных и морфологически нормальных сперматозоидов в эякуляте — ИКС (А) и продолжительности бесплодия при нормозооспермии (Б).
При использовании стимулирующей терапии (кломифена цитртат по 50 мг/сут), традиционно применяемой для лечения гипо- и нормогонадотропных форм секреторного бесплодия, в случае присутствия АСАТ даже в небольших количествах наблюдается тенденция к увеличению MAR%IgG (табл.3). Имеется большой разброс индивидуальных значений MAR в процессе лечения: от снижения на -10% до увеличения на +70%. Количественные показатели спермограммы, за исключением доли сперматозоидов с быстро-поступательным движением (категория А), при этом остаются в пределах статистической ошибки.
| Показатели | Исходные | Лечение | MIN | MAX |
|---|---|---|---|---|
| Объем (мл) | 3.09.0.25 | 3.53.0.33 | -1.4 | +3.8 |
| Концентрация (млн/мл) | 60.5.12.6 | 75.5.11.2 | -56.0 | +117.7 |
| Подвижн. категории А (%) | 5.94.1.26 | 10.9.2.3* | -8.0 | +21.0 |
| Патологических форм (%) | 29.2.4.2 | 33.3.4.8 | -27.0 | +68.0 |
| MAR%IgG | 7.8.0.9 | 14.2.7.7 | -10.0 | +70.0 |
Таблица 3. Основные показатели спермограммы при стимуляции сперматогенеза антиэстрогенами (кломифена цитрат по 50 мг/сут) у мужчин с АСАТ, M.m (n=17)
* — различия до и на фоне лечения достоверны с P
Обсуждение
Таким образом, очевидно, что АСАТ являются патогенетически значимым фактором бесплодия, поскольку соответствуют основным критериям патологии [12]: являются относительно редким явлением с точки зрения статистики (18%), связаны с нарушением мужской репродуктивной функции и поддаются лечению.
Значительно более высокая частота случаев нормозооспермии при наличии АСАТ позволяет считать этот фактор патогенетически важным в отсутствие беременностей даже при нормальных количественных показателях спермограммы.
Наши данные подтверждают, что наличие АСАТ на поверхности большинства сперматозоидов резко ухудшает прогноз на беременность. Это связано с нарушениями подвижности сперматозоидов и их проникновения в цервикальную слизь, преждевременной акросомальной реакцией, с чем, в частности связано, снижение вероятности оплодотворения яйцеклеткой даже in vitro [1-3, 24 и др.]. Даже повышение концентрации свободного Т, которое очевидно носит вторично-компенсаторный характер, не способно предотвратить ухудшение качества спермы.
Как показали представленные выше данные, вероятность наступления беременности статистически снижена даже когда не более 10% подвижных сперматозоидов покрыты АСАТ. При этом количественные показатели спермограммы — концентрация, подвижность и морфология сперматозоидов — могут быть как в пределах нормы (нормозооспермия), так и резко снижены. В последнем случае наиболее вероятной причиной ухудшения качества спермы будет двусторонняя обструкция семявыносящих путей (азооспермия), или односторонние нарушения проходимости, приводящие к более или менее выраженной патоспермии (олиго-, астено-, тератозооспермии). О преобладании обструкции и вторичного внетестикулярного повреждения сперматозоидов над первичными нарушениями сперматогенеза у мужчин с грубыми нарушениями качества спермы на фоне АСАТ свидетельствуют относительно нормальное строение яичек, придатков и физиологичные уровни гонадотропинов.
Как показало сравнение данных, полученных методами MAR и ПЦМ, только доля прогрессивно-подвижных сперматозоидов, покрытых АСАТ классов IgG и IgA отрицательно связаны с продолжительностью бесплодия. Общий процент живых клеток, покрытых IgG, IgA, IgM, имеет обратную корреляцию только с количественными показателями спермограммы. Определение АСАТ с помощью ИФА следует считать недостаточно чувствительным для первичного скрининга, что согласуется с данными литературы [2, 5, 6].
Использование терапии повышает шансы на беременность. Однако снижение величины MAR%IgG, например на фоне применения кортикостероидов, не сопровождается статистически значимым ростом числа беременностей, что показано в т.ч. нашими исследованиями [19, 25, 26]. С другой стороны, при любом способе лечения доля пациентов с исходно низким или высоким процентом АСАТ-позитивных сперматозоидов, от которых наступила беременность, остается примерно одинаковой. Следовательно, вероятность беременности зависит не только от величины MAR%IgG, но и неких других факторов, изучение которых должно продолжаться.
В целом, полученные данные и анализ литературы позволяют сделать вывод, что наличие аутоиммунных реакций против сперматозоидов всегда приводит к снижению вероятности наступления беременности. Нарушения качества спермы и реальной фертильности нарастают с увеличением доли АСАТ-позитивных сперматозоидов. Различия по сравнению с фертильными мужчинами статистически достоверны при любых значениях MAR% IgG>0%. По сравнению с бесплодными без АСАТ, в условиях равенства количественных показателях спермограммы, вероятность наступления беременности у АСАТ-позитивных мужчин становится достоверно меньше при MAR%IgG>50%. Вероятность наступления беременности в естественном цикле без лечения от мужчин с MAR%IgG>50% составляет менее 2%, а при MAR%IgG=100% практически равна 0. Исследование эякулята на наличие АСАТ является обязательным этапом диагностики бесплодных пар. Наличие АСАТ не характерно для хронического неспецифического простатита. Лечение бесплодных мужчин с аутоиммунными реакциями против сперматозоидов требует использования специальных методов лечения независимо от величины MAR%IgG>0%. Неспецифическая стимуляция сперматогенеза у мужчин с АСАТ приводит к усилению аутоиммунного процесса и ухудшению качества спермы.
Иммунологическое бесплодие у мужчин: причины, симптомы, лечение
Иммунологическое бесплодие встречается у 10 % мужчин с диагнозом бесплодие. Так называют заболевание, при котором мужской организм воспринимает собственные сперматозоиды как чужеродные клетки и вырабатывает антиспермальные антитела для их уничтожения.

Иммунологическое бесплодие делает практически невозможным оплодотворение яйцеклетки естественным путем.
Причины иммунологического бесплодия
Иммунологическое бесплодие у мужчин возникает по разным причинам:
- Инфекции мочеполовой системы (ВПЧ, хламидиоз и др.).
- Хронический воспалительный процесс при простатите (воспаление предстательной железы), эпидидимите (воспаление придатков яичек).
- Травмы (сильный удар по мошонке, нижней части живота), хирургическое вмешательство.
- Аномалии строения половых органов (расширение вен семенного канала, отсутствие семявыносящих протоков).
Перечисленные факторы приводят к тому, что естественный гематотестикулярный барьер между семенными протоками и кровью разрушается. В результате сперматозоиды попадают в кровь, где вызывают иммунную реакцию, в результате которой начинают вырабатываться антиспермальные антитела (АСАТ). Они действуют так, как должны действовать антитела при встрече с врагом: покрывают поверхность сперматозоидов, разрушают оболочку сперматозоидов, обездвиживают их, склеивают несколько сперматозоидов между собой. В результате сперматозоиды теряют подвижность, способность проникать через цервикальную слизь и, даже достигнув яйцеклетки, не могут растворить ее оболочку, чтобы попасть внутрь.
Симптомы болезни
Иммунологическое бесплодие редко сопровождается выраженными симптомами. У мужчины нет проблем с эрекцией, поэтому он никак не может узнать о своей проблеме до попыток стать отцом. Обычно об иммунологическом бесплодии узнают, когда пара начинает проходить обследование из-за ненаступления беременности в течение года половой жизни.
Для выявления иммунологического бесплодия делают специальный МАР-тест. Обычная спермограмма не позволяет установить наличие антиспермальных тел.
Лечение иммунологического бесплодия у мужчин
Есть несколько способов лечения. Все они должны способствовать снижению выработки антиспермальных антител. Во-первых, нужно устранить предрасполагающие факторы: вылечить урогенитальные инфекции, купировать хроническое воспаление, после травм – восстановить анатомическую целостность мошонки и т. д.
После этого переходят к следующим этапам лечения. Они могут включать:
- Иммуносупрессивную терапию (подавление нежелательных иммунных реакций со стороны организма).
- Противоаллергическую терапию.
- Системную энзимотерапию (прием противовоспалительных препаратов на основе ферментов животного и растительного происхождения).
Если комплексное лечение не помогает уменьшить выработку АСАТ, а беременность не наступает, врачи предлагают прибегнуть к вспомогательным репродуктивным технологиям (ВРТ). В зависимости от количества АСАТ могут быть выбраны следующие методы:
- ВМИ (внутриматочная инсеминация). Специально подготовленную сперму вводят в матку при помощи катетера. ВМИ делают в день овуляции.
- ЭКО (экстракорпоральное оплодотворение). Оплодотворение яйцеклетки сперматозоидом происходит в лабораторных условиях, затем эмбрион подсаживают в матку. ЭКО используют тогда, когда сперматозоиды способны к зачатию, но не могут достичь яйцеклетки.
- ИКСИ (интрацитоплазматическая микроинъекция). Сперматозоид вводят в яйцеклетку, то есть ему не нужно самостоятельно преодолевать шеечную слизь и растворять оболочку яйцеклетки.
При подготовке к зачатию при помощи ВРТ назначают прием специализированных комплексов для улучшения сперматогенеза, особенно для повышения подвижности и жизнеспособности, а также для увеличения количества сперматозоидов правильного строения. Особенно хорошие показывает Сперотон (подробнее о продукте можно узнать здесь), его эффективность при подготовке к ЭКО клинически доказана. В результате приема Сперотона увеличивается подвижность и количество сперматозоидов, улучшается их строение.
Сегодня даже мужчина с иммунологическим бесплодием может стать отцом, если обратится к специалистам-репродуктологам.
Иммунологическое бесплодие
Иммунологическое бесплодие – гипериммунное состояние женского или мужского организма, сопровождающееся секрецией специфических антиспермальных антител. Иммунологическое бесплодие проявляется несостоятельностью зачатия и наступления беременности при регулярной половой жизни без контрацепции при отсутствии других женских и мужских факторов инфертильности. Диагностика иммунологического бесплодия включает исследование спермограммы, антиспермальных антител плазмы, проведение посткоитального теста, MAR-теста и других исследований. При иммунологическом бесплодии применяются кортикостероиды, методы иммунизации и вспомогательные репродуктивные технологии.
Общие сведения
Иммунологическое бесплодие — наличие патологического антиспермального иммунитета, препятствующего процессу оплодотворения яйцеклетки и имплантации эмбриона. При иммунологическом бесплодии антитела к сперматозоидам – антиспермальные антитела (АСАТ) могут синтезироваться как женским, так и мужским организмом и присутствовать в цервикальной и внутриматочной слизи, сыворотке крови, семенной плазме, семявыводящих протоках. Иммунологический фактор оказывается причиной бесплодия у 5-20% семейных пар в возрасте до 40 лет, при этом АСАТ могут выявляться только у одного супруга или сразу у обоих. Изучением проблемы иммунологического бесплодия занимаются специалисты в области репродуктивной медицины (гинекологи — репродуктологи, андрологи).
В минимальном количестве АСАТ могут присутствовать у фертильных мужчин и женщин, но их фиксация на мембранах большинства сперматозоидов резко ухудшает прогноз на беременность. Это связано с нарушением качества и фертильности спермы — повреждением структуры и резким спадом подвижности сперматозоидов, снижением их способности проникать в цервикальную слизь, блокадой подготовительных стадий (капацитации и акросомальной реакции) и самого процесса оплодотворения яйцеклетки. При наличии АСАТ существенно снижается качество эмбрионов, нарушаются процессы их имплантации в матку, формирования плодных оболочек и развития, что приводит к гибели зародыша и прерыванию беременности на самых ранних сроках.

Причины иммунологического бесплодия
По своей антигенной структуре сперматозоиды являются чужеродными для женского и для мужского организма. В норме они защищены механизмами супрессии иммунного ответа: у мужчин — гемато-тестикулярным барьером (ГТБ) в яичке и его придатке, иммуносупрессивным фактором спермоплазмы и способностью сперматозоидов к мимикрии (к сорбции и десоробции поверхностных антигенов); у женщин — уменьшением уровня Т-хелперов, Ig и С3-компонента системы комплемента, повышением числа Т-супрессоров во время овуляции.
У мужчин
Под действием определенных неблагоприятных факторов нарушение защитных механизмов делает возможным контактирование спермальных антигенов с иммунной системой и приводит к развитию иммунологического бесплодия. Причинами выработки аутоантител на сперматозоиды и клетки сперматогенеза у мужчин могут выступать:
- острые и тупые травмы мошонки и операции на яичках;
- инфекции и воспалительные процессы урогенитального тракта (гонорея, хламидиоз, герпес, ВПЧ, орхит, эпидидимит, простатит);
- врожденные или приобретенные дефекты половых органов (крипторхизм, перекрут яичка, варикоцеле, фуникулоцеле и др.), онкопатология.
У женщин
Сбой внутриматочной иммунной толерантности и появление АСАТ у женщин в предимплантационный период могут быть спровоцированы:
- инфекционно-воспалительными заболеваниями репродуктивного тракта;
- повышенным уровнем лейкоцитов в эякуляте партнера (при неспецифическом бактериальном простатите);
- контактом с иммуногенными сперматозоидами партнера, уже связанными с его аутоантителами;
- попаданием спермы в ЖКТ при оральном/анальном сексе;
- применением химических средств контрацепции;
- коагуляцией эрозии шейки матки в анамнезе;
- нарушениями при внутриматочной инсеминации;
- гормональным «ударом» при попытке ЭКО;
- травмой при заборе яйцеклеток.
Опосредованно стимулировать выработку АСАТ в женском организме могут другие изоантигены, содержащиеся в эякуляте партнера — ферменты и внутриклеточные антигены сперматозоидов, HLA антигены; несовместимость в системах ABO, Rh-Hr, MNSs.
Степень поражения сперматозоидов зависит от класса (IgG, IgA, IgM) и титра АСАТ, места их фиксации, уровня возникновения иммунной реакции. АСАТ, соединяющиеся с хвостовой частью сперматозоидов, затрудняют их движение, а фиксирующиеся к головке — блокируют слияние с ооцитом.
Симптомы иммунологического бесплодия
Иммунологическое бесплодие внешне протекает бессимптомно, не имея видимых проявлений у обоих партнеров. У мужчин с аутоиммунным бесплодием обычно сохраняется активный сперматогенез, эректильная функция и полноценность полового акта. При гинекологическом обследовании женщины не обнаруживаются маточные, трубно-перитонеальные, эндокринные и иные факторы, препятствующие зачатию.
При этом у супружеской пары детородного возраста при условии нормального менструального цикла женщины и регулярной половой жизни без предохранения имеет место отсутствие беременности в течение года и более. При АСАТ у женщин из-за дефекта имплантации и нарушения развития эмбриона наблюдается его гибель и отторжение, прерывание беременности на очень ранних сроках, обычно до того, как женщина может ее обнаружить.
Диагностика иммунологического бесплодия
При бесплодии комплексное обследование необходимо пройти и женщине, и мужчине — у гинеколога и уролога-андролога соответственно. Иммунологический характер бесплодия диагностируют по результатам лабораторных исследований: анализа эякулята, специальных биологических проб — посткоитального теста (Шуварского– унера in vivo и Курцрока–Миллера in vitro), MAR-теста; 1ВТ-теста, ПЦМ. определения антиспермальных антител плазмы. На время проведения диагностических испытаний прием гормональных и других лекарственных препаратов прерывают.
Наличие мужского фактора иммунологического бесплодия можно предположить при нарушении спермограммы (резком падении количества, искажении формы, агглютинации и слабой активности сперматозоидов, низкой выживаемости спермы, полном отсутствии живых спермиев). Данные основного посткоитального теста помогают выявить АСАТ в цервикальной слизи по ее воздействию на подвижность и жизнеспособность сперматозоидов в содержимом шеечного канала. Для соединенных с АСАТ сперматозоидов характерна низкая мобильность и адинамия, маятникообразные движения и феномен «дрожания на месте».
Одновременно со спермограммой выполняется MAR-тест, определяющий количество АСАТ-позитивных подвижных сперматозоидов (при MAR IgG >50% очевиден диагноз «мужское иммунное бесплодие»). 1ВТ-тест устанавливают локализацию АСАТ на поверхности сперматозоида и процент АСАТ-связанных спермиев. Методом проточной цитофлуорометрии (ПЦМ) оценивают концентрацию АСАТ на одном сперматозоиде, спонтанную и индуцированную акросомальную реакцию. При выявлении отклонений в спермограмме и посткоитальном тесте показано проведение ИФА с целью определения спектра АСАТ в сыворотке крови. Дополнительно может проводиться ПЦР-исследование на урогенитальные инфекции (хламидии, микоплазмы, ВПГ, ВПЧ, и др.), определение аутоантител к фосфолипидам, ДНК, кардиолипину, тиреоидным гормонам, HLA-типирование. Иммунологическое бесплодие необходимо дифференцировать от женского и мужского бесплодия другого генеза.
Лечение иммунологического бесплодия
При иммунологическом бесплодии проводят коррекцию иммунного статуса женщины длительными курсами или ударными дозами кортикостероидов, назначают антигистаминные и антибактериальные препараты. В случае аутоиммунных процессов (антифосфолипидный синдром) лечение дополняют низкими дозами аспирина или гепарина. Использование барьерного способа контрацепции (презервативов) в течение 6-8 месяцев с исключением контакта сперматозоидов с иммунными клетками половых органов женщины позволяет уменьшить сенсибилизацию ее организма. Подавление иммунитета повышает шансы зачатия в 50% случаев. Для нормализации иммунных механизмов в женском организме предлагается подкожное введение аллогенных лимфоцитов (мужа/донора) до зачатия или внутривенное введение γ-глобулина — смеси белков плазмы от разных доноров.
Устранение мужского компонента иммунологического бесплодия основано на лечении фоновой патологии, приведшей к образованию АСАТ, и может включать оперативные вмешательства, корригирующие аномалии репродуктивного тракта и кровообращения. Возможно назначение приема протеолитических ферментов, цитостатиков и кортикостероидов.
Основными в лечении иммунологического бесплодия выступают вспомогательные репродуктивные технологии, которые требуют тщательного обследования и подготовки супругов. При искусственной инсеминации осуществляется введение спермы мужа непосредственно в полость матки, минуя шеечный канал, в овуляторном периоде женщины. При наличии способных к оплодотворению, но не достигающих яйцеклетку сперматозоидов, применяется метод искусственного оплодотворения. При низком оплодотворяющем потенциале более высокая частота наступления беременности достигается методом ИКСИ — интрацитоплазматической инъекцией одного качественного сперматозоида в цитоплазму яйцеклетки с последующей подсадкой эмбрионов в полость матки.
Для выхода полноценной яйцеклетки проводится гормональная стимуляция суперовуляции. Получение сперматозоидов у мужчин производят путем эякуляции, биопсии яичка (TESA, TESE, Micro-TESE) или биопсии придатка яичка (PESA, MESA). В тяжелых случаях мужского иммунологического бесплодия используется донорская сперма. Наличие высокого титра АСАТ в крови женщины является противопоказанием для инсеминации, ИКСИ и ЭКО и требует продолжительного лечения до нормализации их уровня. Перспективно при лечении иммунологического бесплодия использование более качественных морфологически селекционных или генетически здоровых и функционально активных сперматозоидов (ИМСИ и ПИКСИ) и предимплантационной выбраковки или обработки эмбрионов (ассистированный хэтчинг). Для повышения вероятности наступления беременности производится предимплантационная криоконсервация эмбрионов.
Иммунологическое бесплодие имеет достаточно специфический характер: АСАТ вырабатываются на сперматозоиды конкретного мужчины, и при смене партнера появляется возможность беременности. При полноценном лечении с использованием современных ВРТ иммунологическое бесплодие удается преодолеть в большинстве нетяжелых случаев. Вероятность беременности в естественном цикле в отсутствие лечения мужчины с MAR IgG > 50% составляет
Источник https://www.cironline.ru/articles/92482/
Источник https://plan-baby.ru/statyi/immunologicheskoe-besplodie-u-muzhchin-prichiny-simptomy-lechenie
Источник https://www.krasotaimedicina.ru/diseases/zabolevanija_gynaecology/immunological-infertility